
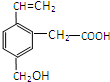
 某有机物的结构如图所示,这种有机物不可能具有的性质是
某有机物的结构如图所示,这种有机物不可能具有的性质是| A. | ①④ | B. | 只有⑥ | C. | 只有③ | D. | ④⑥ |
分析 该物质中含有碳碳双键、苯环、羧基和醇羟基,具有烯烃、苯、羧酸和醇的性质,能发生加成反应、加聚反应、氧化反应、还原反应、中和反应、酯化反应、取代反应等,据此分析解答.
解答 解:①含有碳碳双键和羟基,可被酸性KMnO4溶液氧化,故正确;
②为烃的含氧衍生物,可以燃烧生成二氧化碳和水,故正确;
③含有碳碳双键,羧基和羟基,不能发生水解反应,故错误;
④含有羧基和羟基,能发生酯化反应,故正确;
⑤含有碳碳双键,能发生加聚反应,故正确;
⑥含有羧基,具有酸性,能跟NaOH溶液反应,故正确.
故选C.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查烯烃、羧酸、醇的性质,注意:该物质还能发生缩聚反应,题目难度不大.


科目:高中化学 来源: 题型:解答题
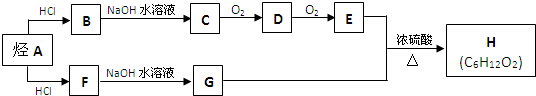
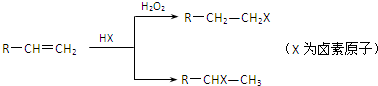
 CH3CH2COOCH(CH3)2+H2O.
CH3CH2COOCH(CH3)2+H2O. .(用结构简式表示)
.(用结构简式表示)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z | W |
| A. | X、Y、Z、W四种元素均为非金属元素 | |
| B. | Y、W的最简单氢化物中,Y的沸点高 | |
| C. | X、Y、Z、W最高价氧化物均为共价化合物 | |
| D. | W元素的简单离子半径小于Z元素的简单离子半径 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 方法 | 目的 | 离子方程式 | |
| A | 中和法 | 用H2SO4中和碱性废水 | H++OH-═H2O |
| B | 混凝法 | 除去水中悬浮物 | Al3++H2O═Al(OH)3↓+H+ |
| C | 沉淀法 | 除去废水中的Hg2+ | Hg2++Na2S═HgS↓+Na+ |
| D | 氧化法 | 消毒 | Cl2+2OH-═Cl-+ClO-+H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
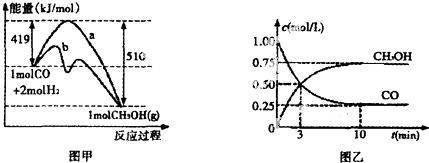
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 的电离程度分别用α1、α2表示,则α1小于α2(填“大于”、“小于”、“等于”或“无法确定”)
的电离程度分别用α1、α2表示,则α1小于α2(填“大于”、“小于”、“等于”或“无法确定”)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com