
��15�֣�ʵ�����������᳧����(��Ҫ�ɷ�Ϊ���������P����FeS��SiO2��)�Ʊ�����(��ʽ�������ľۺ���)���̷�(FeSO4��7H2O)���������£�
��1�������̢��еIJ���������ͨ��������Һ�У���Һ����ɫ���� ��
A��Ʒ����Һ B����ɫʯ����Һ C������KMnO4��Һ D����ˮ
��2�����̢��У�FeS��O2��H2SO4��Ӧ�����ӷ���ʽΪ�� ��
��3�����̢��У������������� ��
��4�����̢��У������ᾧ��Ҫʹ�þƾ��ơ����Ǽܡ������ǣ�����Ҫ�������� ��
��5�����̢ݵ���pH��ѡ�������Լ��е� (��ѡ�����)��
A��ϡ���� B��CaCO3 C��NaOH��Һ
��6�����̢��У�����ҺZ���ȵ�70һ80�棬Ŀ���� ��
��7��ʵ����Ϊ�������õ��ľ�����Ʒ����Ԫ�ص�������������������ʵ�顣���÷�����ƽ��ȡ2.700g��Ʒ���ڽ���Ʒ�����������������������Ȼ�����Һ���۹��ˡ�ϴ�ӡ�����������ù�������Ϊ3.495g�����þ�����Ҫ�ɷ�Ϊ[(Fe(OH)(SO4)]n����þ�����Ʒ����Ԫ�ص���������Ϊ ��(���������в�����Ԫ�غ���Ԫ��)��
��1��ACD ��2��4FeS+3O2 + 12H+= 4Fe3++6H2O+4S ��3��Fe(����) ��4������������
��5��C��6���ٽ�Fe3+��ˮ�� ��7��31.1%
���������������1������W�к���S��SiO2,�������ա����е�S���ΪSO2���壬SO2������Ư���ԣ���ʹƷ����Һ��ɫ��SO2�����л�ԭ�ԣ���ʹ����KMnO4��Һ����ˮ����������Ӧ��Ӧ����ɫ������ʹ��ɫʯ����Һ��Ϊ��ɫ�����ѡ��ΪA��C��D����2�����̢��У����ݿ�ͼ�еĸ������ʼ������غ㶨�ɺ͵����غ㡢����غ��֪��FeS��O2��H2SO4��Ӧ�����ӷ���ʽΪ4FeS+3O2 + 12H+= 4Fe3++6H2O+4S����3�����ڷ�����Ӧ�õ��������к���Fe3+.�������Ҫ��ȡ�̷�FeSO4�����Թ��̢��У�Ҫ���뻹ԭ��Fe�ۡ���4�����̢��У������ᾧ��Ҫʹ�þƾ��ơ����Ǽܡ������ǣ�����Ҫ����������������������5�����̢ݵ���pH��ʹ��Һ��pH����Ӧ�ü����ų�A����������CaCO3���������ᣬ�����������������Ca2+�����׳�ȥ����˿�ѡ�������Լ��е�NaOH��ѡ��ΪC����6�����̢��У�����ҺZ���ȵ�70һ80�棬Ŀ���Ǵٽ�Fe3+��ˮ��ʹѸ�ٲ�����������7��n(SO42-)=3.495g��233g/mol=0.015mol��n(Fe)= n(SO42-)= 0.015mol,����m(Fe)=0.015mol��56g/mol=0.84g�����Ըþ�����Ʒ����Ԫ�ص���������Ϊ��0.84g�� 2.700g����100%=31.1%��
���㣺����SO2�����ʡ����ӷ���ʽ����д����ѧʵ�����������Ԫ�ص����������ļ����֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ʴ���
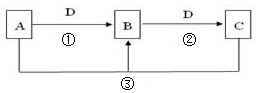
��1����A����������ˮ������D�����������������������;���Ľ������ʣ���������B����Һ���ܵõ�B����B�Ļ�ѧʽ������ ����ҵ����ȡA�����ӷ���ʽ��Ϊ ��
��2����A��һ�ּ������壬�������������B������β��֮һ�����������ɫ����Ӧ�ٵĻ�ѧ����ʽΪ ��
��3����D���ȼҵ����Ҫ��Ʒ��B�����ԣ���Ӧ�ڵ����ӷ���ʽ�� ��
��4����A��C��D���dz������壬C���γ��������Ҫ���壬��Ӧ�۵Ļ�ѧ����ʽ ��
��5���ȼҵ�Ǹߺ��ܲ�ҵ��һ�ֽ�������ȼ�ϵ������ϵ��¹��տ��Խڣ��磩��30%���ϣ������ֹ�������У�������ϵĴ�����ת����ϵ����ͼ��ʾ�����еĵ缫δ��������õ�����Ĥ��ֻ����������ͨ����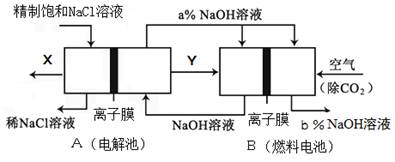
��6�����ͼ��X��Y�ֱ��� ���ѧʽ���������Ƚ�ͼʾ������������������a% b%�����������=��������
��д��ȼ�ϵ��B�и����Ϸ����ĵ缫��Ӧ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
����һ�Թ�NO2��ijͬѧ������±�ʵ�飬�Ծ����ܶ��ʹNO2��ˮ���ա�
��������±���
| ʵ�鲽�� | ʵ������ | ���ͣ��û�ѧ����ʽ��ʾ�� | |
| �� | ������NO2�ĵ�����ʢ��ˮ��ˮ���У���ȥ��Ƥ��������ζ��Թܡ� | �Թ�����������������ɫ��Ϊ��ɫ��Һ���������Թܸ߶ȵ�����������ܿڣ����� | |
| �� | | | |
| �� | �ظ�����ڵIJ������Σ�ֱ��Һ����������Թܡ� | �Թ��ڳ�����ɫҺ�塣 | �ܷ�Ӧ����ʽ�� |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��16�֣�ij�о�С�����о�̼��Ũ����ķ�Ӧ����ʵ��������¡�
| ���� | ���� |
| a���ø���ྻ���ձ�ȡԼ10 mLŨ���ᣬ���ȡ� | |
| b����С���պ��ľ̿Ѹ�������ȵ�Ũ�����С� | ���ȵ�ľ̿���ȵ�Ũ����Ӵ��������ҷ�Ӧ��ͬʱ�д�������ɫ���������Һ����ľ̿Ѹ��ȼ�գ����������� |
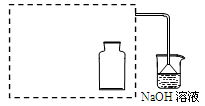
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
ij��ѧ�С���������ͼ��ʾ(���ּг�װ������ȥ)ʵ��װ�ã���̽����ʪ��Cl2��Na2CO3��Ӧ�õ��Ĺ������ʡ�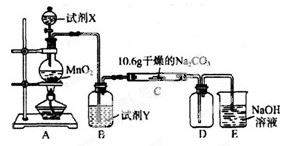
��1��д��װ��A�з�����Ӧ�����ӷ���ʽ�� ��
��2��д���Լ�Y������_____________________��
��3����֪��ͨ��һ�������������D��ֻ��һ�ֳ�����Ϊ�ƺ�ɫ�����壬��Ϊ�������������ȷ������C�к��е�����ֻ��һ�֣��Һ���NaHCO3���ֶ�C�ɷֽ��в����̽����
������������裺
����һ���������ֳɷ֣�NaHCO3��__________
��������������ֳɷ֣�NaHCO3��__________��__________��
����Ʒ���������ʵ�顣��д��ʵ�鲽���Լ�Ԥ������ͽ��ۣ��ɲ���������
��ѡʵ���Լ�������������ˮ��ϡ���ᡢBaCl2��Һ������ʯ��ˮ��AgNO3��Һ���Թܡ�С�ձ���
| ʵ�鲽�� | Ԥ������ͽ��� |
| ����1��ȡC�е�����������Ʒ���Թ��У��μ���������ˮ�������ܽ⣬Ȼ��������Һ�ֱ�����A��B�Թ��С� | |
| ����2����A�Թ��еμ�_________�� | ��������������֤�������в���̼���ƣ� ������Һ����ǣ�֤�������к���̼���ơ� |
| ����3����B�Թ��еμ�________�� | ����Һ����ǣ���ϲ���2�еĢ٣������һ��������ϲ���2�еĢڣ������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
Ϊ��̽��AgNO3�����ȶ��ԣ�ij��ѧ��ȤС�����������ʵ�顣����ͼ��ʾ��ʵ��װ��A����AgNO3���壬��������ɫ���壬��װ��D���ռ�����ɫ���塣����Ӧ�������Թ��в�������Ϊ��ɫ��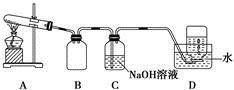
(1)װ��B�������� ��
(2)��С�����۲���֤����ɫ����ΪO2������֤������ ��
(3)���������ϡ�Ag2O�ͷ�ĩ״��Ag��Ϊ��ɫ��Ag2O�����ڰ�ˮ��
��������롿�Թ��в����ĺ�ɫ��������ǣ���.Ag����.Ag2O����.Ag��Ag2O��
��ʵ����֤����С��Ϊ��֤�������룬�ֱ�ȡ������ɫ��������Թ��У�����������ʵ�顣
| ʵ���� | ���� | ���� |
| a | ����������ˮ���� | ��ɫ���岻�ܽ� |
| b | ��������ϡ���ᣬ�� | ��ɫ�����ܽ⣬����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�������һ����Ҫ�ķǽ������ϣ��Ʊ��������Ҫ�������£�
�ٸ������ù�����̼��ԭ���������Ƶôֹ裬ͬʱ�õ�һ�ֿ�ȼ�����壻
�ڴֹ�������HCl���巴Ӧ�Ƶ�SiHCl3(Si��3HCl SiHCl3��H2)��
SiHCl3��H2)��
��SiHCl3�������H2��1 100��1 200 ����¶��·�Ӧ�Ƶô��裬��֪SiHCl3����ˮ���ҷ�Ӧ���ڿ���������ȼ��
��ش�
(1)��һ����ȡ�ֹ�Ļ�ѧ��Ӧ����ʽΪ ��
(2)�ֹ���HCl���巴Ӧ��ȫ�������õ���SiHCl3(�е�33.0 ��)�к�������SiCl4(�е�57.6 ��)��HCl(�е㣭84.7 ��)���ᴿSiHCl3���õķ���Ϊ ��
(3)ʵ������SiHCl3�������H2��Ӧ��ȡ����װ����ͼ��ʾ(���Ⱥͼг�װ����ȥ)��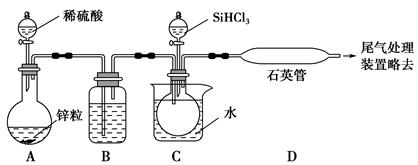
��װ��B�е��Լ��� ��װ��C�е��ձ���Ҫ���ȣ�Ŀ���� ��
�ڷ�Ӧһ��ʱ���װ��D�й۲쵽�������� ��װ��D���ܲ�����ͨ�����ܵ�ԭ���� ��װ��D�з�����Ӧ�Ļ�ѧ����ʽ�� ��
��Ϊ��֤�Ʊ�����ʵ��ijɹ��������Ĺؼ��Ǽ��ʵ��װ�õ������ԣ����ƺ÷�Ӧ�¶��Լ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
CaCO3�㷺��������Ȼ�磬��һ����Ҫ�Ļ���ԭ�ϡ�����ʯ��Ҫ�ɷ�ΪCaCO3�������������ĺ����ʵ�����ô���ʯ��ϡ���ᷴӦ�Ʊ�CO2���塣����װ�ÿ�����CO2������ᴿ���
���������գ�
(1)��Ũ��������1��1(�����)��ϡ����(Լ6 mol��L��1)��Ӧѡ�õ������� ��
a���ձ� b�������� c����Ͳ d������ƿ
(2)����װ���У�A�� ��NaHCO3��Һ�������� ��
(3)����װ���У�B������ �������ʵ��õ�������ⶨCO2����Է������������B����ʧЧ���ⶨ��� (�ƫ�ߡ�����ƫ�͡�����Ӱ�족)��
(4)һ���Է�����ʯ��(������)��CaCO3��ʳ���е��ܳ��������۷���������ָ��֮һ���ⶨ�ܳ�������Ҫʵ�鲽��������£�
���顢���ء������ܽ�����ˡ�������ɡ���ȴ�����ء�����
Ϊ�˽�ʯ����̼����ܳ���Ӧѡ�õ��Լ��� ��
a���Ȼ�����Һ b��ϡ���� c��ϡ���� d��������
(5)���ܳ����ⶨʵ���У�Ϊ�˻��ʯ����̼��Ƶ�����ܳ�����Ӧ���ܳ� �����ܳ� ��
(6)�����ⶨʵ���У����� ��˵����Ʒ�Ѿ����ء�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
ij�о���ѧϰС���ͬѧΪ��֤Ũ������ͭ�ܷ�Ӧ��ϡ����ܣ��������ͼ��ʾװ�ý���̽������6.4 gͭƬ�ͺ�0.2 moL���ʵ�18.4 mol/LŨ�������Բ����ƿ�й��ȣ�ֱ������������Ϊֹ�����ٶ��ڴ˹�����Һ������䣩
��1����ͬѧ��ΪҪ֤ʵ�������ۣ���Ӧ����ϡ������ͭƬ��ϼ���ʵ�飬����Ϊ���ޱ�Ҫ����˵�����ɣ�________________
��2�������Լ����ܹ�������һ��֤����Ӧ���������ƿ��ȷ��������ǣ�_____
| A������ | B���� | C���Ȼ�����Һ | D������ |
| ��� | ��������ԭ�� | ��� ��ƫ�ͻ�ƫ�ߣ� | �ı��ʩ |
| ������ | | | |
| ������ | | | |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com