
| A. | NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-═CO32-+H2O | |
| B. | 氯化亚铁溶液和稀硝酸混合:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑ | |
| C. | AlCl3溶液中加入足量的氨水:Al3++4OH-═AlO2-+2H2O | |
| D. | NO2溶于水:3NO2+H2O═2H++2NO3-+NO |
分析 A.漏掉氨根离子与氢氧根离子的反应;
B.氯化亚铁溶液和稀硝酸混合,硝酸将二价铁离子氧化生成三价铁离子;
C.不符合反应客观事实,应生成氢氧化铝;
D.NO2溶于水反应生成硝酸和一氧化氮.
解答 解:A.NH4HCO3溶于过量的NaOH溶液中,离子方程式:NH4++HCO3-+2OH-═CO32-+H2O+NH3•H2O,故A错误;
B.将氯化亚铁溶液和稀硝酸混合,反应生成铁离子和一氧化氮气体,反应的离子方程式为:3Fe2++4H++NO3-═3Fe3++2H2O+NO↑,故B正确;
C.AlCl3溶液中加入足量的氨水,离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故C错误;
D.NO2溶于水,离子方程式:3NO2+H2O═2H++2NO3-+NO,故D正确;
故选:AC.
点评 本题考查了离子方程式的书写,掌握离子方程式的书写原则,明确反应实质是解题关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | (1)(2)(3)(4)(5) | B. | (3)(1)(4)(2)(5) | C. | (5)(1)(3)(2)(4) | D. | (5)(4)(3)(2)(1) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素代号 | W | R | X | Y | Z |
| 原子半径/nm | 0.037 | 0.154 | 0.066 | 0.070 | 0.077 |
| 主要化合价 | +1 | +1 | -2 | -3、+5 | +2、+4 |
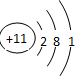
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
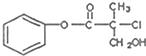
| A. | 该有机物可以在一定条件下与HBr发生反应 | |
| B. | 1mol该有机物最多能与4molH2发生加成反应 | |
| C. | 该有机物在一定条件下可以发生消去反应 | |
| D. | 1mol该有机物一足量的NaOH溶液反应,最多可以消耗3molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
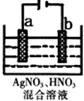 化学反应原理在生活和工业中应用广泛.
化学反应原理在生活和工业中应用广泛.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C02分子比例模型示意图: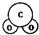 | B. | O原子核外电子轨道表示式: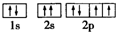 | ||
| C. | Ca2+电子排布式:ls22s23s23p6 | D. | K原子结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
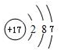 .②的氢化物含有化学键的类型是共价键,与②的氢化物分子所含电子总数相等的分子是H2O(举一例、填化学式,下同)、离子是OH-.
.②的氢化物含有化学键的类型是共价键,与②的氢化物分子所含电子总数相等的分子是H2O(举一例、填化学式,下同)、离子是OH-.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com