
下列说法正确的是
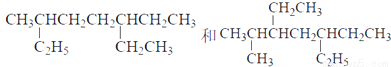
A.主链碳原子数均为7个
B.主链含5个碳原子,有甲基、乙基2个支链的烷烃有三种
C. 新戊烷、正丁烷、异丁烷和丙烷的熔沸点依次降低
D.C7H16的烷烃中,含有3个甲基的同分异构体有2种
C
【解析】
试题解析:主链是含碳数最多的碳链,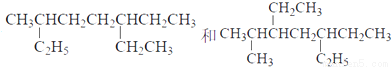 ,主链碳原子数分别为8个、7个,故A错误;主链含有5个碳原子,则取代基只能连在直接2、3、4号碳原子上,且乙基连在3号碳原子上,即分别是相邻或相对,所以共有2种同分异构体,故B错误;碳数越多,烷烃熔沸点越高,同碳数时,支链越多,烷烃熔沸点越低,则新戊烷、正丁烷、异丁烷和丙烷的熔沸点依次降低,故C正确;该烃结构式中含有3个甲基,则该烷烃只有1个支链,若支链为-CH3,主链含有6个碳原子,符合条件有:CH3CH(CH3)CH2CH2CH2CH3,CH3CH2CH(CH3)CH2CH2CH3;若支链为-CH2CH3,主链含有5个碳原子,符合条件有:CH3CH2CH(CH2CH3)CH2CH3;支链不可能大于3个碳原子,故符合条件的烷烃有3种,故D错误。
,主链碳原子数分别为8个、7个,故A错误;主链含有5个碳原子,则取代基只能连在直接2、3、4号碳原子上,且乙基连在3号碳原子上,即分别是相邻或相对,所以共有2种同分异构体,故B错误;碳数越多,烷烃熔沸点越高,同碳数时,支链越多,烷烃熔沸点越低,则新戊烷、正丁烷、异丁烷和丙烷的熔沸点依次降低,故C正确;该烃结构式中含有3个甲基,则该烷烃只有1个支链,若支链为-CH3,主链含有6个碳原子,符合条件有:CH3CH(CH3)CH2CH2CH2CH3,CH3CH2CH(CH3)CH2CH2CH3;若支链为-CH2CH3,主链含有5个碳原子,符合条件有:CH3CH2CH(CH2CH3)CH2CH3;支链不可能大于3个碳原子,故符合条件的烷烃有3种,故D错误。
考点:同分异构体


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源:2015届青海省西宁市高三上学期第一次月考理综化学试卷(解析版) 题型:填空题
选考题[化学—选修2:化学与技术](15分)
硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸。
(1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,反应的化学方程式为: ,该反应在 中进行(填仪器名称)。
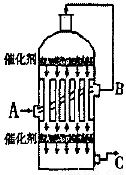
(2)为了有利于SO2转化为SO3,且能充分利用热能,采用了多层催化剂且有热交换器的 (填仪器名称)中进行反应。在如图所示的装置中,C处流出的气体有 ;SO3进入 (填仪器名称)用 吸收,得到浓硫酸或发烟硫酸。
(3)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据下表信息,
结合工业生产实际,选择最合适的生产条件是 。

(4)现在欲提高SO2的反应速率和转化率,下列措施可行的是 。
A、向装置中通入氮气且保持体积不变
B、向装置中通入氧气且保持体积不变
C、添加更多的催化剂
D、降低温度,及时转移SO3
(5)由吸收塔排出的尾气中有SO2的含量如果超过500μL/ L,就要加以处理后才能排出,处理方法之一是用氨水洗涤烟气脱硫,用方程式表示氨水洗涤吸收塔排除的尾气的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2015届陕西省高二下学期期末考试化学试卷(解析版) 题型:选择题
实验法和比较法是研究物质性质的基本方法。以下实验设计中不合理或不严密的是
A.钠和镁分别与冷水反应,判断钠和镁的金属性强弱
B.测定相同温度下盐酸和醋酸溶液的pH,就可证明盐酸是强酸、醋酸是弱酸
C.铁分别与氯气和硫反应,判断氯气与硫的氧化性强弱
D.测定相同条件下Na2CO3溶液和Na2SO4溶液的pH,判断碳与硫的非金属性强弱
查看答案和解析>>
科目:高中化学 来源:2015届重庆市高三上期第一次月考理综化学试卷(解析版) 题型:选择题
/在T℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g/cm3,溶质的质量分数为 ,物质的量浓度为c mol/L。则下列选项不正确的是
,物质的量浓度为c mol/L。则下列选项不正确的是
A.溶质的质量分数为 B.用水稀释该溶液,OH-的物质的量增加
B.用水稀释该溶液,OH-的物质的量增加
C.该溶液中共有6种微粒 D.上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5ω
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高二上学期期中考试化学试卷(解析版) 题型:填空题
某研究小组为测定某软锰矿中MnO2的质量分数,查阅资料获得如下信息:KMnO4、MnO2在酸性条件下均能将草酸钠(Na2C2O4)氧化,反应过程表示为:
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O,MnO2+C2O42-+4H+=Mn2++2CO2↑+2H2O
小组成员采用滴定的方法测定软锰矿中MnO2的质量分数,设计实验如下:准确称取2.20g软锰矿样品,加入2.68g草酸钠固体,再加入足量的稀硫酸并加热(杂质不参加反应),充分反应之后冷却、滤去杂质,将所得溶液转移到100mL容量瓶中并定容;从中分别取出20.00mL待测液置于锥形瓶中,再用0.0200mol·L-1KMnO4标准溶液进行滴定,记录最终读数。数据如下:
测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
初始读数(mL) | 0.40 | 0.10 | 0.90 | 0.00 |
最终读数(mL) | 25.05 | 20.10 | 21.00 | 19.90 |
试回答下列问题:
(1)0.0200mol·L-1KMnO4标准溶液应置于 (选填“酸式”或“碱式”)滴定管中;滴定终点如何判断 。
(2)你能否帮助该研究小组求得软锰矿中MnO2的质量分数 (选填“能”或“否”)。若回答“能”,请给出计算结果 (保留小数点后两位);若回答“否”,试说明原因 。
(3)若在实验过程中存在下列操作,其中会使所测MnO2的质量分数偏小的是 。
A.溶液转移至容量瓶中,未将烧杯、玻棒洗涤
B.滴定前尖嘴部分有一气泡,滴定终点时消失
C.定容时,俯视刻度线
D.滴定前仰视读数,滴定后俯视读数
E.锥形瓶水洗之后未用待测液润洗
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高二上学期期中考试化学试卷(解析版) 题型:选择题
甲烷和丙烷混和气的密度与同温同压下一氧化碳的密度相同,混和气中甲烷和丙烷的体积比是
A.4:3 B.3:4 C.2:1 D.1:1
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高二上学期期中考试化学试卷(解析版) 题型:选择题
已知某温度下水的离子积KW=3.4×10-15.取该温度下浓度相同的NaOH和HCl溶液,以3∶2体积比相混合,所得溶液的pH等于12,则原溶液的浓度为
A.0.01mol·L-1 B.0.017mol·L-1
C.0.05mol·L-1 D.0.50mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省高一上学期期中考试化学试卷(解析版) 题型:选择题
下列十二种物质中:Fe、 CaO、SO3、盐酸、硫酸、KOH溶液、NH4HCO3、CCl4、NH3·H2O 、HF、BaSO4、熔融的KCl. 其中属于强电解质、弱电解质、非电解质的物质种类依次为:
A.5、2、2 B.7、3、2 C.6、2、4 D.5、3、4
查看答案和解析>>
科目:高中化学 来源:2015届辽宁省分校高三上学期期初考试化学试卷(解析版) 题型:填空题
(6分)氯化铜晶体(CuCl2·2H2O)含有FeCl2杂质,为制得纯净氯化铜晶体,首先将其制成水溶液,然后按下列操作步骤进行提纯:
①先加入氧化剂X,再加入物质Y,过滤得沉淀Z;
②将滤液蒸发结晶得纯CuCl2·2H2O晶体。
已知:三种离子从溶液中完全呈氢氧化物沉淀所需pH值:Fe3+:3.7,Cu2+:6.4,Fe2+:6.4试回答下列问题:
(1)加入氧化剂X的原因是____ __。
(2)下列物质都可以作为氧化剂,其中最适宜于本实验的是( )
A.H2O2 B.KMnO4 C.NaClO D.K2CrO7
(3)物质Y是__ ____,沉淀Z是__ ____.
(4)为分离出沉淀Z,采取的实验操作所用仪器有__ ____。
(5)操作②所用的仪器有____ __。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com