
下列说法或表示方法中正确的是( )
A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多
B.由C(金刚石)→C(石墨)ΔH= -1.9KJ/mol 可知,金刚石比石墨稳定
C.由2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1可知,H2的燃烧热为-571.6 kJ·mol-1
D.稀溶液中:H+(aq)+OH—(aq)=H2O(l) ΔH= —53.7KJ/mol ,若将含0.5 molH2SO4的浓溶液与含1 molNaOH的溶液混合,放出的热量大于57.3KJ
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案科目:高中化学 来源: 题型:
在指定的条件下,下列各组离子能大量共存的是( )
A.使甲基橙变红的溶液中:Fe2+、Na+、I-、NH4+
B.强碱性溶液中:K+、Na+、ClO-、S2-
C.0.1 mol·L-1 NaAlO2溶液中:H+、Na+、Cl-、SO42-
D.由H2O电离出的c(H+)=10-11mol/L溶液中:Na+、HCO3-、AlO2-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
有人建议将氢元素排在元素周期表的第ⅦA族。下列事实能支持这一观点的是( )
①氢原子得到一个电子后最外层电子达到稳定结构 ②氢分子的结构式为H—H
③与碱金属元素形成离子化合物M+[∶H]- ④分子中原子间的化学键都属于非极性键
A.①②③ B.①③④ C.②③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E五种短周期元素,其原子序数依次增大,而原子半径按A、C、B、E、D
顺序依次增大。A、D同主族;B、D、E三种元素原子的最外层电子数之和为10;E的单
质可做半导体材料;C与E两元素形成的化合物可与A、C、D形成的化合物Y发生反应;
B元素的气态氢化物与其最高价氧化物的水化物可以发生反应生成化合物M。1molM中含
有42mol电子。回答下列问题:
(1) E元素在周期表中的位置 ;化合物M中含有的化学键类型有
(2)比较B、C、E形成的气态氢化物的稳定性由强到弱的顺序是
(用化学式表示);写出C与A形成的18e-化合物的电子式 ,
该化合物类型为 (填“共价化合物”或“离子化合物”)
(3)写出C与E两元素形成的化合物与Y溶液反应的离子方程式
;写出题中生成M的化学方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
A.原子的电子层数越多,原子半径越大
B.同族元素相差的原子序数可能为16、26、36、46
C.ⅠA族与ⅦA族元素间可形成共价化合物或离子化合物
D.卤族元素的单质均有氧化性,最高正价都是+7
查看答案和解析>>
科目:高中化学 来源: 题型:
柠檬酸的结构简式如图,下列说法正确的是
A.柠檬酸中能发生酯化反应的官能团有2种
B.1 mol柠檬酸可与4 mol NaOH发生中和反应
C.1 mol柠檬酸与足量金属Na反应生成生成1.5 mol H2
D.柠檬酸与O2在Cu作催化剂,加热的条件下,能发生氧化反应
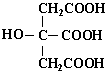 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com