
发射卫星用N2H4作燃料,NO2作氧化剂,两者反应生成N2和水蒸气,
已知:N2(g)+O2(g)=2NO2(g)△H1=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g)△H2=﹣534kJ/mol
试写出N2H4与 NO2反应的热化学方程式 .
考点:
热化学方程式;用盖斯定律进行有关反应热的计算.
专题:
化学反应中的能量变化.
分析:
依据热化学方程式的意义和盖斯定律的内容通过合并计算得到热化学方程式.
解答:
解:①N2(g)+O2(g)=2NO2(g)△H1=+67.7kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H2=﹣534kJ/mol
依据盖斯定律:②×2﹣①得到:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=﹣1135.7KJ/mol;
故答案为:2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=﹣1135.7KJ/mol.
点评:
本题考查了热化学方程式的书写方法和盖斯定律的计算应用,题目较简单.


科目:高中化学 来源: 题型:
金属铝质轻且有良好的防腐蚀性,在国防工业中有非常重要的作用。请完成下列空白:
(1)铝元素在周期表中的位置为________。
(2)在19世纪时,铝是一种珍贵的金属。人们最初得到的铝粒如同珍宝,它的价格同黄金 相当。1827年,德国化学家维勒用金属钾与无水氯化铝反应而制得了金属铝。用钾与无水氯化铝反应制铝而不用氯化铝溶液的理由是_________。
现代工业炼铝的原料是由铝土矿提取而得,在提取过程中通入的气体为____。
(3)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高 温下煅烧,所得物质可作耐高温材料,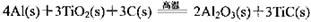
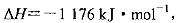 则反应过程中,每转移1 mol电子放出的热量为________。
则反应过程中,每转移1 mol电子放出的热量为________。
(4)硅与铝同周期,地壳里硅铝的含量:硅________铝(填>,<或=)。是硅酸盐玻璃 (Na2CaSi6O14)的主要成分,Na2CaSi6O14也可写成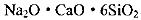 。盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式 ________。长石是铝硅盐酸,不同类长石其氧原子的物质的量分数相同。由钠长石化学式NaAlSi3O8可推知钙长石的化学式为________。
。盛放NaOH溶液的试剂瓶若用玻璃瓶塞容易形成粘性的硅酸盐而无法打开,发生反应的化学方程式 ________。长石是铝硅盐酸,不同类长石其氧原子的物质的量分数相同。由钠长石化学式NaAlSi3O8可推知钙长石的化学式为________。
(5)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如: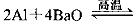
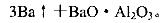 利用化学平衡移动原理解释上述方法可制取金属Ba的原因是
利用化学平衡移动原理解释上述方法可制取金属Ba的原因是
_____________________________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
下图表示的是难溶氢氧化物在不同pH下的溶解度(S,mol/L),下列说法中正确的是( )
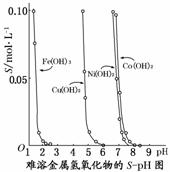
A.pH=3时溶液中铁元素的主要存在形式是Fe3+
B.若Ni(NO3)2溶液中含有少量的Co2+杂质,可通过调节溶液pH的方法来除去
C.若分离溶液中的Fe3+和Cu2+,可调节溶液的pH在4左右
D.若在含有Cu2+和Ni2+的溶液中加入烧碱,Ni(OH)2优先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CH3CH2CH2CH3(g)+6.5O2(g)═4CO2(g)+5H2O(l)△H=﹣2878kJ•mol﹣1,(CH3)2CHCH3(g)+6.5O2(g)═4CO2(g)+5H2O(l)△H=﹣2869kJ•mol﹣1下列说法正确的是( )
|
| A. | 正丁烷分子储存的能量大于异丁烷分子 |
|
| B. | 正丁烷的稳定性大于异丁烷 |
|
| C. | 异丁烷转化为正丁烷的过程是一个放热过程 |
|
| D. | 异丁烷分子中的碳氢键比正丁烷的多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个带有理想活塞(即无质量、无摩擦力的刚性活塞)的体积可变的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g)⇌A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡.下列说法中正确的是( )
|
| A. | 平衡时C的转化率:乙>甲 | B. | 平衡时C的体积分数:乙>甲 |
|
| C. | 反应速率:乙>甲 | D. | 平衡时A的物质的量:甲>乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列属于正确的水解离子方程式的是( )
|
| A. | NH4++H2O⇌NH3•H2O+H+ | B. | H2O+H2O⇌H3O++OH﹣ |
|
| C. | CO32﹣+2H2O⇌H2CO3+2OH﹣ | D. | Fe3++3H2O⇌Fe(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
在密闭容器中进行如下反应:X(g)+Y(g)⇌2Z(g),已知X、Y、Z的起始浓度分别为0.1mol/L、0.2mol/L、0.2mol/L,在一定条件下,达到平衡时,各物质的浓度不可能是( )
|
| A. | Z为0.3 mol/L | B. | Y为0.15 mol/L |
|
| C. | X为0.1 mol/L | D. | Z为0.4 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
按要求书写
(1)H2CO3的电离方程式
(2)NaHSO3的电离方程式
(3)NH4Cl水解的离子方程式
(4)向Na2CO3溶液中滴加酚酞呈红色的原因是 (用离子方程式表示); 溶液中各离子浓度由大到小的顺序 ;向此溶液中加入AlCl3溶液,观察到的现象是 ,反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
有以下几种物质①熔融氯化钠 ②浓硫酸 ③Cu ④蔗糖 ⑤CH3COOH ⑥NaHCO3 ⑦酒精 ⑧液溴,填空回答:(填序号)
(1)以上物质中属于强电解质的是 ; 属于非电解质的是 ;
(2)写出⑤⑥在水中的电离方程式:⑤ ;⑥ .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com