
| A、甲苯和水 | B、甲苯和苯 |
| C、溴乙烷与水 | D、苯与溴乙烷 |
科目:高中化学 来源: 题型:
| A、1:2 | B、1:3 |
| C、1:6 | D、3:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素的性质随着原子序数的递增而呈周期性变化 |
| B、随着元素原子序数的递增,原子最外层电子数总是从1到8重复出现 |
| C、随着元素原子序数的递增,元素的最高化合价从+1到+7,最低化合价从-7到-1重复出现 |
| D、元素性质的周期性变化是指相对原子量的周期性变化、原子半径的周期性变化及元素主要化合价的周期性变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸性:H2SiO3<H2SO4<HClO4 |
| B、碱性:NaOH>Mg(OH)2>Al(OH)3 |
| C、稳定性:HCl>H2S>PH3 |
| D、还原性:F->Cl->Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol/L |
| B、2mol/L |
| C、3 mol/L |
| D、4 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:Be<B<C<N |
| B、第一电离能:B<Be<Mg<Na |
| C、元素的电负性:O>N>S>P |
| D、气态氢化物的稳定性:NH3<CH4<PH3<SiH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
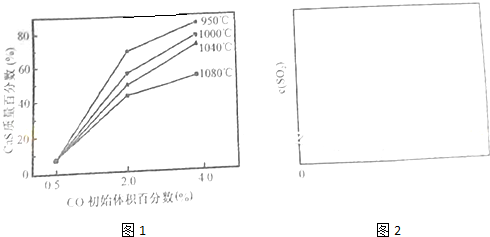
查看答案和解析>>
科目:高中化学 来源: 题型:
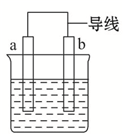 如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:
如图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com