
下图所示各物质间的转化关系中,A、B是两种钠盐,均含有同一种非金属元素。

请根据图示关系,回答下列问题:
(1)写出下列物质的化学式:沉淀③ ,溶液⑨(溶质) 。
(2)写出下列反应的离子方程式:
②→⑥ 。
⑦→④ 。
(3)混合溶液①中的两溶质A和B可能存在多种组合,将其可能的组合中A和B的化学式及其物质的量nA、nB间应满足的数学关系式填入下表中(任填二种)
| 组合 | A | B | nA和nB的关系 |
| I | |||
| II |
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:北京市海淀区2009届高三年级第一学期期中练习化学试题 题型:022
A和R在一定条件下可合成芳香族化合物E,已知A可以在一定条件下转化为G,且G在标准状况下密度为1.25 g/L.各物质间相互转化关系如下图所示(某些条件已略去).
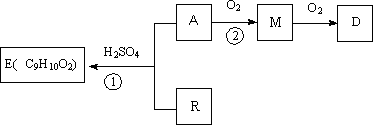
(1)A中所含官能团的名称为________;①的反应类型为________.
(2)②的化学反应方程式为________.
M与新制氢氧化铜悬浊液反应的化学方程式________.
(3)与E具有相同官能团,且苯环上只有一个取代基的同分异构体还有5种,它们是:
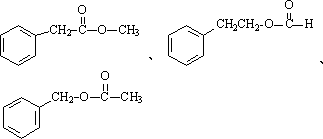
________、________.
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省肇庆市高三第二次高考模拟理综化学试卷(解析版) 题型:计算题
合成氨然后再生产尿素是最重要的化工生产。
I.在3个2 L的密闭容器中,在相同的温度下、使用相同的催化剂分别进行反应:
3H2(g) + N2(g) 2NH3(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
2NH3(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如下:
|
|
甲 |
乙 |
丙 |
|
反应物投入量 |
3 mol H2、2 mol N2 |
6 mol H2、4mol N2 |
2 mol NH3 |
|
达到平衡的时间/min |
|
5 |
8 |
|
平衡时N2的浓度/mol·L-1 |
c1 |
1.5 |
|
|
NH3的体积分数 |
ω1 |
|
ω3 |
|
混合气体密度/g·L-1 |
ρ1 |
ρ2 |
|
(1)容器乙中反应从开始到达平衡的反应速率为v(H2)=___________。
(2)在该温度下甲容器中反应的平衡常数K= (用含c1的代数式表示)。
(3)分析上表数据,下列关系正确的是________(填序号):
a.2c1 > 1.5 b.2ρ1 = ρ2 c.ω3 = ω1
II.工业上用氨气合成尿素(H2NCONH2)的反应在进行时分为如下两步:
第一步:2NH3(l)+CO2(g) H2NCOONH4 (l) (氨基甲酸铵)
△H1
H2NCOONH4 (l) (氨基甲酸铵)
△H1
第二步:H2NCOONH4(l) H2O(l)+H2NCONH2(l)
△H2
H2O(l)+H2NCONH2(l)
△H2
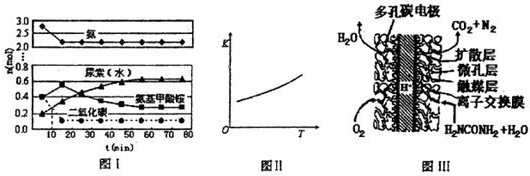
(4)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如左下图I所示:

①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第 步反应决定。
②第二步反应的平衡常数K随温度T的变化如右上图II所示,则△H2 0;③若第一步反应升温时氨气浓度增大,请在图II中画出第一步反应K1随温度T变化曲线,并作出必要的标注。
(5)氨和尿素溶液都可以吸收硝工业尾气中的NO、NO2,将其转化为N2。
①尿素与NO、NO2三者等物质的量反应为:CO(NH2)2+NO+NO2 =CO2+2N2+2H2O
该反应中的氧化剂为 (写化学式)。
②已知:N2(g)+O2(g)= 2NO(g) △H =a kJ·mol-1
N2(g)+3H2(g)= 2NH3(g) △H2=bkJ· kJ·mol-1
2H2(g)+O2(g)= 2H2O(g) △H = c kJ·mol-1
则4NH3(g) +4NO(g) +O2(g)= 4N2(g)+6H2O(g) △H= 。
③尿素燃料电池结构如下图所示。其工作时负极电极反应式可表示为 。

查看答案和解析>>
科目:高中化学 来源: 题型:
A和R在一定条件下可合成芳香族化合物E,已知A可以在一定条件下转化为G,且G在标准状况下密度为1.25 g/L。各物质间相互转化关系如下图所示(某些条件已略去)。

(1)A中所含官能团的名称为 ;①的反应类型为 。
(2)②的化学反应方程式为 。M与新制氢氧化铜悬浊液反应的化学方程式 。
(3)与E具有相同官能团,且苯环上只有一个取代基的同分异构体还有5种,它们是:
 、
、  、
、 
_________ _、 。
查看答案和解析>>
科目:高中化学 来源: 题型:
A和R在一定条件下可合成芳香族化合物E,已知A可以在一定条件下转化为G,且G在标准状况下密度为1.25 g/L。各物质间相互转化关系如下图所示(某些条件已略去)。

图5
(1)A中所含官能团的名称为 ;①的反应类型为 。
(2)②的化学反应方程式为 。
C与新制氢氧化铜悬浊液反应的化学方程式 。
(3)与E具有相同官能团,且苯环上只有一个取代基的同分异构体还有5种,它们是:
 、
、  、
、 
_________ _、 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com