
| A、NH4Cl溶液中:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
| B、Na2SO4溶液中:c(Na+)+c(H+)=c(SO42-)+c(OH-) |
| C、NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-) |
| D、浓度均为0.1mol?L-1CH3COOH与CH3COONa溶液等体积混合:2c(H+)-2c(OH-)=c (CH3COO-)-c(CH3COOH) |


科目:高中化学 来源: 题型:

| A、容器I、Ⅲ中平衡常数相同 |
| B、容器II、Ⅲ中正反应速率始终相同 |
| C、容器Ⅱ、Ⅲ中的反应达平衡时,SO3的体积分数:II>III |
| D、容器I中SO2的转化率与容器Ⅱ中SO3的转化率之和等于1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
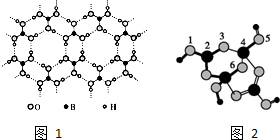 硼酸晶体具有层状结构,每一层的结构结构如图1所示.
硼酸晶体具有层状结构,每一层的结构结构如图1所示.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、往溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,则该溶液中一定含有NH4+ |
| B、往溶液中加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,则该溶液中一定含有Ba2+ |
| C、用铂丝蘸取溶液放在酒精灯上灼烧,观察火焰为黄色,则该溶液中一定含Na+而不含K+ |
| D、往溶液中加入少量氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则该溶液中一定含有SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶液中被沉淀的离子 | Fe3+ | Fe2+ | Cu2+ |
| 完全生成氢氧化物沉 淀时,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
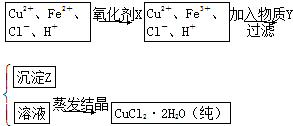
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、16 gCH4与18 gNH4+所含质子数相等 |
| B、CH4O和C2H6O都符合CnH2n+2O的通式,它们可能互为同系物 |
| C、32S与33S的质子数相等,属于同一种元素的不同原子 |
| D、质量相等、体积不等的N2和C2H4的分子数一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是七个基本物理量之一 |
| B、氮气的摩尔质量是28g |
| C、0.5mol氢气的体积为11.2L |
| D、1molH2O约含有6.02×1023个水分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Kw值随温度升高而增大 |
| B、纯水中,25℃时,c(H+)?c(OH-)=1×10-14 |
| C、25℃时,任何以水为溶剂的稀溶液中c(H+)?c(OH-)=1×10-14 |
| D、蒸馏水中,c(H+)?c(OH-)=1×10-14 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com