
【题目】向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
选项 | 操作及现象 | 结论 |
A | 加入AgNO3溶液,生成白色沉淀,再加稀盐酸沉淀不溶解 | 原溶液中有Cl-存在 |
B | 通入Cl2后,溶液变为深黄色,继续加入淀粉溶液后溶液变蓝 | 原溶液中有I-存在 |
C | 加入Ba(NO3)2溶液,生成白色沉淀,加稀盐酸后沉淀不溶解时 | 原溶液中有 |
D | 加入稀盐酸,生成的气体能使澄清石灰水变浑浊 | 原溶液中有 |
A.AB.BC.CD.D
【答案】B
【解析】
A.在加入盐酸之前生成的可能是AgCl沉淀也可能是碳酸银沉淀等等,但是后面加入盐酸后可以转化为AgCl,所以沉淀不溶解,因此,不能确定原溶液里是否有Cl-是存在,A错误;
B.氯气能将碘离子氧化为碘单质,碘水溶液为棕黄色,碘遇淀粉变蓝色,B正确;
C.硝酸根在酸性条件下有强氧化性。若溶液中含有亚硫酸根或亚硫酸,加入Ba(NO3)2溶液后,都能生成白色沉淀,加稀盐酸酸化后,亚硫酸钡能被硝酸根氧化成硫酸钡,因此,不能确定原溶液中是否有硫酸根离子存在,C错误;
D.碳酸根、碳酸氢根、亚硫酸根、亚硫酸氢根遇到盐酸,均会生成能使澄清石灰水变浑浊的气体,因此,不能确定原溶液中有碳酸根离子,D错误;
答案选B。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】用活性炭还原氮氧化物可防止空气污染。向1L密闭容器加入一定量的活性炭和NO,某温度下发生反应:
已知:①C(s)+2NO(g)![]() N2(g)+CO2 (g) ΔH
N2(g)+CO2 (g) ΔH
②C(s)+O2(g)![]() CO2 (g) ΔH1= -393.5 kJ/mol
CO2 (g) ΔH1= -393.5 kJ/mol
③N2(g)+O2(g)![]() 2NO(g) ΔH2= +180.5 kJ/mol
2NO(g) ΔH2= +180.5 kJ/mol
下列说法错误的是
A.ΔH= -574.0 kJ/mol
B.当容器内气体密度不变时,反应①达到平衡状态
C.反应③正反应的活化能大于180.5 kJ/mol
D.反应①达到平衡后,增大压强平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面有关晶体的叙述中,不正确的是( )
A.金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子
B.氯化钠晶体中,每个Na+周围距离相等且紧邻的Na+共有6个
C.氯化铯晶体中,每个Cs+周围紧邻8个Cl-
D.干冰晶体中,每个CO2分子周围紧邻12个CO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
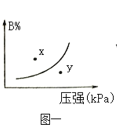

A.图一表示反应:mA(s)+nB(g)![]() pC(g)△H>0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的慢.
pC(g)△H>0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的慢.
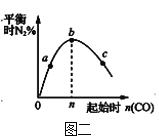
B.图二表示反应2CO(g)+2NO(g)![]() N2(g)+2CO2(g),在其他条件不变时,改变起始CO的物质的量,平衡时N2的体积分数变化,由图可知NO的转化率b>c>a
N2(g)+2CO2(g),在其他条件不变时,改变起始CO的物质的量,平衡时N2的体积分数变化,由图可知NO的转化率b>c>a
C.图三表示对于化学反应mA(g)+nB(g)![]() pC(g)+qD(g),A的百分含量与温度(T)的变化情况,则该反应的ΔH>0。
pC(g)+qD(g),A的百分含量与温度(T)的变化情况,则该反应的ΔH>0。
D.图四所示图中的阴影部分面积的含义是(v正-v逆)
查看答案和解析>>
科目:高中化学 来源: 题型:
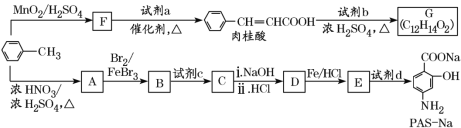
【题目】以甲苯为原料合成某种食用香料(有机物G)和某种治疗肺结核药物的有效成分(有机物PASNa)的路线如下:
已知:①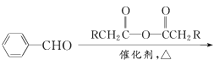
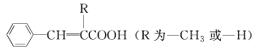
②![]()
③![]()
回答下列问题:
(1)肉桂酸中所含官能团的名称是______________。
(2)①试剂a的结构简式是________________。
②写出由A生成B的化学方程式:____________________。
(3)已知试剂b为相对分子质量为60的醇,且无支链,写出G的结构简式:________________,由肉桂酸制取G的反应类型是________。
(4)①当试剂d过量时,可以选用的试剂d是_____(填字母)。
a.NaOH b.Na2CO3 c.NaHCO3
②参照题中信息,设计以![]() 为起始原料制备
为起始原料制备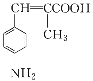 的合成路线。
的合成路线。
____________________。
(5)在肉桂酸分子中碳碳双键催化加氢后得到化合物X(分子式为C9H10O2),X有多种同分异构体,符合下列条件的有________种。写出其中一种处于对位且核磁共振氢谱中比例为6:1:2:2:1的结构简式______________________________。
a.苯环上有两个取代基
b.能发生银镜反应
c.与Na作用有H2产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A.在NH4Al(SO4)2溶液中滴加少量烧碱溶液:Al3++4OH-=![]() +2H2O
+2H2O
B.在含等物质的量浓度的Na2CO3和NaOH溶液中滴加过量的盐酸:![]() +OH-+2H+=
+OH-+2H+=![]() +H2O
+H2O
C.在Mg(HCO3)2溶液中滴加过量的澄清石灰水:Mg2++2![]() +2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O
+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O
D.在Fe(NO3)2稀溶液中滴加少量NaHSO4溶液:Fe2++![]() +2H+=Fe3++NO2↑+H2O
+2H+=Fe3++NO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室进行1,2-二溴乙烷的消去反应,按下列步骤进行,请填空:

(1)按图连接好仪器装置并___。
(2)在试管a中加入2 mL 1,2-二溴乙烷和5 mL 10% NaOH的___溶液,再向试管中加入几片___。
(3)在试管b中加少量溴水。
(4)用水浴法加热试管里的混合物,持续加热一段时间后,把生成的气体通入溴水中,观察到的现象是____。
(5)①写出发生反应的化学方程式:__________。
②本实验中应注意的问题有______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.Na与H2O的反应是熵增的放热反应,该反应能自发进行
B.饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同
C.FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同
D.Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)![]() Mg2+(aq)+2OH—(aq),该固体可溶于NH4Cl溶液
Mg2+(aq)+2OH—(aq),该固体可溶于NH4Cl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的氧化物和氮的氢化物的任意排放均会对环境造成污染,因此关于其转化的研究对于消除环境污染有着重要意义。
(1)已知T℃时,有如下反应:
反应I:4NH3(g) + 6NO(g)![]() 5N2 ( g) + 6H2O(g) △H = -1804 kJmol-1
5N2 ( g) + 6H2O(g) △H = -1804 kJmol-1
反应II:N2(g) +2O2(g) ![]() 2NO2(g) △H = +67.8 kJmol-1
2NO2(g) △H = +67.8 kJmol-1
反应III:2NO(g) + O2 (g) ![]() 2 NO2 (g) △H =-116.2 kJmol-1
2 NO2 (g) △H =-116.2 kJmol-1
试写出T℃ 时,NH3与NO2反应生成不污染环境的物质的热化学反应方程式 ______。
(2)T℃时,向2L密闭容器中加入一定量的NO2、NO和O2,发生(1)中反应III,不同时间测得各物质的部分浓度(molL-1) 如下表所示:
时间( min) | NO | O2 | NO2 |
0 | a | 0.30 | 0.10 |
10 | 0.14 | 0.27 | b |
20 | 0.10 | c | 0.20 |
30 | d | 0.24 | 0.22 |
40 | 0.08 | e | f |
①温度不变,反应达平衡后容器中的压强与最初加入气体时的压强之比为_______。
②反应的前 20 min 的平均反应速率v(NO)=________molL-1·min-1。
③若温度不变,平衡后将反应容器压缩为1L,达到新的平衡后,c(O2)_____0.48molL-1(填“>”“<”或“ =”)。
(3)某化学兴趣小组利用电解原理设计实验消除NH3 与 NO对环境的影响, 并制取KOH溶液和H2SO4溶液,其工作原理如下图所示:
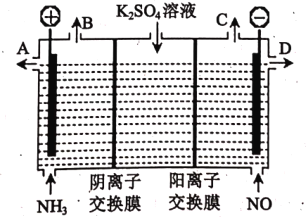
①从出口B、C产生的气体相同,该气体是_____:从出口 D 得到的溶液是____。
②电解槽左池中发生的电极反应式为________ 。
③电解一段时间,两电极共收集到22.4L气体(标准状况下)时,理论上将生成____________mol KOH。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com