
【题目】己烯雌酚是一种激素类药物,结构如图,下列有关叙述中不正确的是![]()
![]()
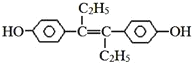
A.该有机物在一定条件下能发生加聚反应和氧化反应
B.该有机物可与NaOH和Na2CO3发生反应
C.1mol该有机物可以与5molBr2发生反应
D.该有机物分子中,最多有16个碳原子共平面
科目:高中化学 来源: 题型:
【题目】下列溶液中的c(SO42-)与50mL1mol·L-1Al2(SO4)3溶液中的c(SO42-)相等的是
A. 150mL1mol·L-1Na2SO4溶液
B. 75mL2mol·L-1(NH4)2SO4溶液
C. 150mL3mol·L-1K2SO4溶液
D. 20mL1.5mol·L-1Fe2(SO4)3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NOx会造成大气污染,在工业上采用多种方法进行处理。
I.氧化法:烟气中的NO经O3预处理后转化为NO2,再用CaSO3悬浊液吸收NO2。
已知:常温下,CaSO4的沉淀溶解平衡常数数值为9.1×10-6,CaSO3的沉淀溶解平衡常数数值为3.1×10-7。
(1)NO与O3反应过程的能量变化如下:
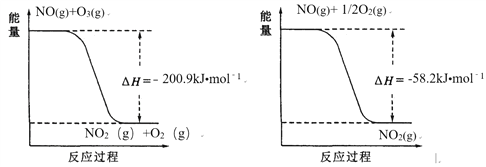
NO被O3氧化的总反应是化合反应,该反应的热化学方程式为 ________。
(2)将CaSO3悬浊液静置,取上层清液,测得pH约为8,用化学用语解释其原因为________。
(3)用CaSO3悬浊液吸收NO2,将其转化为HNO2,该反应的化学方程式为________。
(4)在实际吸收NO2的过程中,通过向CaSO3悬浊液中加入Na2SO4固体,提高NO2的吸收速率,从溶解平衡的角度解释其原因:________。
II. 选择性非催化还原法:该反应不使用催化剂,但必须在高温有氧下利用NH3做还原剂与 NOx 进行选择性反应:4NH3 + 4NO + O2 ![]() 3N2 + 6H2O,不同温度(T)下,反应时间(t)与NO浓度的关系如右图所示。
3N2 + 6H2O,不同温度(T)下,反应时间(t)与NO浓度的关系如右图所示。
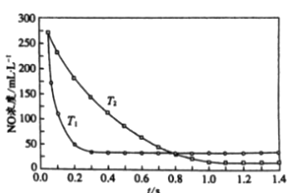
(5)判断该反应为________(填“吸热”或“放热”)反应,说明理由:________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,可逆反应X(s)+Y(g) W(g)+Z(g)△H>0,在一定体积不变的容器中反应达到平衡后,改变条件,反应速率(υ)随时间变化的情况如图所示。下列条件的改变与图中情况相符的是 ( )
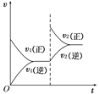
A.增加了X的物质的量B.降低了温度
C.增大了压强D.增大了Y的物质的量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的天然提取和人工合成往往得到的是混合物,假设给你一种这样的有机混合物让你研究,一般要采取的几个步骤是( )
A.分离、提纯![]() 确定化学式
确定化学式![]() 确定最简式
确定最简式![]() 确定结构式
确定结构式
B.分离、提纯![]() 确定最简式
确定最简式![]() 确定化学式
确定化学式![]() 确定结构式
确定结构式
C.分离、提纯![]() 确定结构式
确定结构式![]() 确定最简式
确定最简式![]() 确定化学式
确定化学式
D.确定化学式![]() 确定最简式
确定最简式![]() 确定结构式
确定结构式![]() 分离、提纯
分离、提纯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种重要的化工原料,被广泛应用在工农业生产中。请运用所学知识解决下列问题:
是一种重要的化工原料,被广泛应用在工农业生产中。请运用所学知识解决下列问题:
已知反应:![]()
![]()
![]()
![]() 工业制取炭黑的方法之一是将甲烷隔绝空气加热到
工业制取炭黑的方法之一是将甲烷隔绝空气加热到![]() 进行裂解。该反应的热化学方程式为______。
进行裂解。该反应的热化学方程式为______。
![]() 容积固定为1L的密闭容器内充入
容积固定为1L的密闭容器内充入![]() 和
和![]() ,保持
,保持![]() 发生反应
发生反应![]() ,用压力计监测反应过程中容器内压强的变化如下表:
,用压力计监测反应过程中容器内压强的变化如下表:
反应时间 | 0 | 5 | 10 | 15 | 20 | 25 |
压强 |
|
|
|
|
|
|
则反应从开始到20min时,以CO浓度变化表示的平均反应速率![]() ______。
______。
![]() 对于反应
对于反应![]() 来说:
来说:
![]() 时,平衡常数
时,平衡常数![]() 。
。![]() 测得密闭容器中各物质达到平衡时物质的量浓度分别为:
测得密闭容器中各物质达到平衡时物质的量浓度分别为:![]() ,
,![]() ,
,![]() ,
,![]() ,则
,则![]() ______
______![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() ,判断依据是______。
,判断依据是______。
![]() 下列措施有利于提高反应混合气中
下列措施有利于提高反应混合气中![]() 含量的是______。
含量的是______。
A.使用催化剂 ![]() 升高温度
升高温度 ![]() 及时导出CO
及时导出CO![]() 增大反应体系的压强
增大反应体系的压强
![]() 一定条件下,将
一定条件下,将![]() 与
与![]() 按物质的量之比1:1置于恒容密闭容器中反应,下列能说明该反应达到平衡状态的是______。
按物质的量之比1:1置于恒容密闭容器中反应,下列能说明该反应达到平衡状态的是______。
A.![]()
![]()
B.体系中混合气体密度不变
C.![]() 与
与![]() 的转化率相等
的转化率相等
D.![]() 与
与![]() 物质的量之比不再改变
物质的量之比不再改变
E.反应体系压强不再改变
![]() 以甲烷为燃料的新型电池得到广泛应用。下图是甲烷燃料电池工作原理的示意图。
以甲烷为燃料的新型电池得到广泛应用。下图是甲烷燃料电池工作原理的示意图。
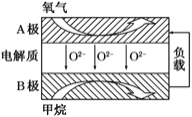
![]() 极上的电极反应式为______。
极上的电极反应式为______。
![]() 以该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到
以该燃料电池作电源,用石墨作电极电解硫酸铜溶液,当阳极收集到![]() 标准状况
标准状况![]() 气体时,消耗甲烷的体积为______
气体时,消耗甲烷的体积为______![]() 标准状况
标准状况![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知碳碳单键可以绕键轴旋转,某烃结构简式可表示为CH3![]()
![]() ,下列说法中正确的是( )
,下列说法中正确的是( )
A.分子中最多有22个原子处于同一平面上
B.该烃苯环上的一氯代物只有一种
C.分子中至少有10个碳原子处于同一平面上
D.该烃是苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车用汽油的抗爆剂约含 17%的 1,2一二溴乙烷。某学习小组用下图所示装置制备少量 1,2 一二溴乙烷,具体流秳如下: 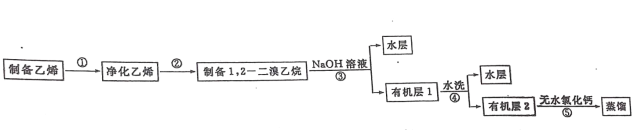
已知:1,2 一二溴乙烷的沸点为131℃,熔点为9.3℃。Ⅰ1,2 一二溴乙烷的制备步聚①、②的实验装置为:

实验步骤:
(ⅰ)在冰水冷却下,将 24mL 浓硫酸慢慢注入12mL乙醇中混合均匀。
(ⅱ)向 D 装置的试管中加入3.0mL 液溴(0.10mol),然后加入适量水液封,幵向烧杯中加入冷却剂。
(ⅲ)连接仪器并检验气密性。向三口烧瓶中加入碎瓷片,通过滴液漏斗滴入一部分浓硫酸与乙醇的混合物,一部分留在滴液漏斗中。
(ⅳ)先切断瓶C与瓶D的连接处,加热三口瓶,待温度上升到约120℃,连接瓶 C与瓶D,待温度升高到180~200℃,通过滴液漏斗慢慢滴入混合液。
(V)继续加热三口烧瓶,待D装置中试管内的颜色完全褪去,切断瓶C与瓶D的连接处,再停止加热。回答下列问题:
(1)图中 B 装置玻璃管的作用为__________________________________________。
(2)(ⅳ)中“先切断瓶C与瓶D的连接处,再加热三口瓶”的原因是__________________________________________。
(3)装置D的烧杯中需加入冷却剂,下列冷却剂合适的为__________________________________________。
a.冰水混合物 b.5℃的水 c.10℃的水
Ⅱ1,2 一二溴乙烷的纯化
步骤③:冷却后,把装置 D 试管中的产物转移至分液漏斗中,用 1%的氢氧化钠水溶液洗涤。
步骤④:用水洗至中性。
步骤⑤:“向所得的有机层中加入适量无水氯化钙,过滤,转移至蒸馏烧瓶中蒸馏,收集
130~132℃的馏分,得到产品5.64g。
(4)步骤③中加入 1%的氢氧化钠水溶液时,发生反应的离子方程式为__________________________________________。
(5)步骤⑤中加入无水氯化钙的作用为_________________________。该实验所得产品的产率为__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某混合气体由两种气态烃组成,取标况下![]() 该混合气体完全燃烧后得到
该混合气体完全燃烧后得到![]() 二氧化碳
二氧化碳![]() 气体已折算为标准状况
气体已折算为标准状况![]() 和10.8g水,则这两种气体可能是
和10.8g水,则这两种气体可能是
A.![]() 和
和![]() B.
B.![]() 和
和![]() C.
C.![]() 和
和![]() D.
D.![]() 和
和![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com