
| A、1mol?L-1的K2SO4溶液中有2NA个K+ |
| B、1mol Cl2与足量铁反应,转移2NA个电子 |
| C、标准状况下,22.4L氨气溶于水,此溶液中含有NA个NH3分子 |
| D、所含溶质为63g的浓硝酸与足量的铜反应,生成的气体分子数为0.5NA |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| c(NH4+) |
| c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、①④ | C、①③ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、装置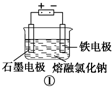 工业上可用于生产金属钠,电解过程中石墨电极产生金属,此法也可用于生产活泼金属镁、铝等 工业上可用于生产金属钠,电解过程中石墨电极产生金属,此法也可用于生产活泼金属镁、铝等 |
B、装置 中随着电解的进行左边电极会产生红色的铜,并且电流表示数不断变小 中随着电解的进行左边电极会产生红色的铜,并且电流表示数不断变小 |
C、装置 中的离子交换膜只允许阳离子、阴离子和小分子水通过 中的离子交换膜只允许阳离子、阴离子和小分子水通过 |
D、装置 的待镀铁制品应与电源正极相连 的待镀铁制品应与电源正极相连 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、42He比32He是同种原子的不同表示形式 |
| B、32He和42He互为同位素 |
| C、32He原子核内含有2个中子 |
| D、42He与32He的质量数相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、③④⑤ |
| C、②③④ | D、②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用过氧化氢从酸化的海带灰浸出液中提取碘:2I-+H2O2+2H+═I2+2H2O | ||||
| B、硝酸银溶液中滴加过量氨水:Ag++NH3?H2O═AgOH↓+NH4+ | ||||
| C、碳酸氢钠的水解:HCO3-+H2O?CO32-+H3O+ | ||||
D、用惰性电极电解氯化镁溶液:2Cl-+2H2O
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强电解质溶液的导电能力比弱电解质强 |
| B、难溶盐如:BaSO4、CaCO3、AgCl等是弱电解质,易溶性盐如:醋酸铵是强电解质 |
| C、在水溶液中是否完全电离是判断强弱电解质的依据 |
| D、二氧化硫溶于水可以导电,所以二氧化硫是电解质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com