
| A. | 苯酚钠溶液中通入CO2: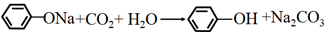 | |
| B. | 常温下CH2=CHCH3与水接触:CH2=CHCH3+H2O→CH3CH(OH)CH3 | |
| C. | 乙醇和金属钠发生反应放出氢气:2CH3CH2OH+2 Na→2CH3CH2ONa+H2↑ | |
| D. | 甲苯与氯气在铁粉催化作用下发生反应: |
分析 A.苯酚的酸性大于碳酸氢根离子,二者反应生成碳酸氢钠;
B.没有催化剂,丙烯与水不发生反应;
C.乙醇与金属钠反应生成CH3CH2ONa和氢气;
D.甲苯与氯气在铁粉催化作用下,应该是苯环氢被取代.
解答 解:A.碳酸的酸性比苯酚的酸性强,所以苯酚钠通入二氧化碳生成苯酚和碳酸氢钠,反应的化学方程式为:C6H5ONa+CO2+H2O→C6H6OH+NaHCO3,故A错误;
B.常温下CH2=CHCH3与水接触,没有催化剂,二者不发生反应,无法书写化学方程式,故B错误;
C.乙醇和金属钠发生反应放出氢气,反应的化学方程式为:2CH3CH2OH+2 Na→2CH3CH2ONa+H2↑,故C正确;
D.甲苯与氯气在铁粉催化作用下发生反应,Cl原子取代的是苯环上的H,如: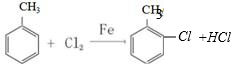 ,故D错误;
,故D错误;
故选C.
点评 本题考查了化学方程式的正误判断,为高考的高频题,题目难度中等,注意掌握化学方程式的书写原则,明确化学方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确等,试题有利于提高学生的规范答题能力.


科目:高中化学 来源: 题型:实验题
| 实验 编号 | 温度 (℃) | 催化剂 用量(g) | 酸性高锰酸钾溶液 | |
| 体积(mL) | 浓度(mol/L) | |||
| 1 | 25 | 0.5 | 4.00 | 0.1000 |
| 2 | 50 | 0.5 | 4.00 | 0.1000 |
| 3 | 25 | 0.5 | 4.00 | 0.0100 |
| 4 | 25 | 0 | 4.00 | 0.1000 |
| 实验 编号 | 溶液褪色所需时间(min) | ||
| 第 1 次 | 第 2 次 | 第 3 次 | |
| 1 | 14.0 | 13.0 | 11.0 |
| 2 | 6.5 | 6.7 | 6.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:H3PO4>H2SO4>HClO4 | B. | 碱性:Mg(OH)2>Ca(OH)2>KOH | ||
| C. | 热稳定性:H2S>H2O>HF | D. | 氧化性:F2>Cl2>Br2>I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量.图是部分元素原子的第一电离能I1随原子序数变化的曲线图.
第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量.图是部分元素原子的第一电离能I1随原子序数变化的曲线图.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 离子组 | 试剂X | 离子方程式 |
| A | Fe3+、Al3+、SiO32-、NO3- | 过量的盐酸 | SiO32-+2H+=H2SiO3↓ |
| B | 透明溶液中:Fe3+、NH4+、SO42-、Cl- | 过量的铜粉 | 2Fe3++Cu=2Fe2++Cu2+ |
| C | Na+、Ba+、HCO3-、Cl- | NaHSO4溶液 | H++HCO3-=CO2↑+H2O |
| D | pH=1的溶液中:Mg2+、Fe2+、NO3-、SO42- | 双氧水 | 2Fe2++H2O2+2H+=2Fe3++2H2O |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R可能为乙二酸 | |
| B. | N可能为对苯二甲酸 | |
| C. | 高聚物M为加聚产物 | |
| D. | 含有羧基的物质在常温下均易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
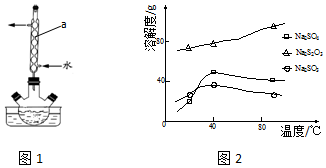
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com