
分析 浓硫酸增重为燃烧生成水的质量,固体质量的过氧化钠发生反应:2CO2+2Na2O2 =2Na2CO3+O2,固体质量增重等于与二氧化碳等物质的量的CO的质量,令乙烷、丙烷的物质的量分别为xmol、ymol,根据C、H原子守恒列方程计算解答.
解答 解:浓硫酸增重为燃烧生成水的质量,其物质的量=$\frac{3.06g}{18g/mol}$=0.17mol,
固体质量的过氧化钠发生反应:2CO2+2Na2O2 =2Na2CO3+O2,固体质量增重等于与二氧化碳等物质的量的CO的质量,故CO的物质的量=$\frac{3.36g}{28g/mol}$=0.12mol,则原混合物中含有0.12mol碳原子,
设乙烷、丙烷的物质的量分别为xmol、ymol,
则:$\left\{\begin{array}{l}{6x+8y=0.17×2}\\{2x+3y=0.12}\end{array}\right.$,
解得:x=0.03、y=0.02,
混合气体中乙烷和丙烷的体积比=0.03mol:0.02mol=3:2,
故答案为:3:2.
点评 本题考查混合物计算,题目难度不大,关键是根据固体质量增重计算C原子物质的量,注意利用原子守恒进行解答,试题培养了学生的分析能力及化学计算能力.


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 乳浊液 | B. | 溶液 | C. | 胶体 | D. | 悬浊液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
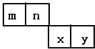 m、n、x、y四种主族元素在周期表里的相对位置如图所示,已知它们的原子序数总和为46,则:
m、n、x、y四种主族元素在周期表里的相对位置如图所示,已知它们的原子序数总和为46,则: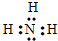 ,空间构型为三角锥形.
,空间构型为三角锥形.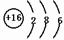 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 金属冶炼和处理常涉及氧化还原反应.
金属冶炼和处理常涉及氧化还原反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置.其材料除单晶硅,还有铜铟镓硒等化合物.
太阳能电池是通过光电效应或者光化学效应直接把光能转化成电能的装置.其材料除单晶硅,还有铜铟镓硒等化合物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | MnO2与浓HCl作用:MnO2+4HCl(浓)$\stackrel{△}{→}$MnCl2+Cl2↑+2H2O | |
| B. | KMnO4+16HCl(浓)→2KCl+2MnCl2↑+5Cl2↑+8H2O | |
| C. | KClO3+6HCl(浓)→KCl+3Cl2↑+3H2O | |
| D. | Ca(ClO)2+4HCl(浓)→CaCl2+2Cl2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
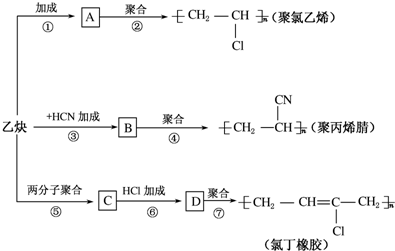

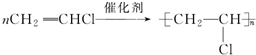 ;
;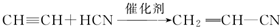 ;
;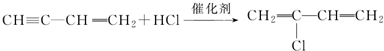 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应I 恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应II 绝热恒容 | 0min | 0 | 0 | 2 | 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com