
【题目】A、B的结构简式如下
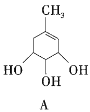
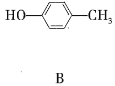
(1)A分子中含有的官能团的名称是__________;B分子中含有的官能团的名称是___________。
(2)A能否与氢氧化钠溶液反应?__________(填“能”或“不能”,下同);B能否与氢氧化钠溶液反应?________。
(3)A在浓硫酸作用下加热可得到B,其反应类型是________________。
(4)A、B各1mol分别加入足量浓溴水,完全反应后消耗单质溴的物质的量分别是______ mol、______mol。
【答案】醇羟基、碳碳双键 酚羟基 不能 能 消去反应 1 2
【解析】
(1)由A、B的结构简式可知,A中无苯环,官能团是醇羟基、碳碳双键,B中有苯环,羟基直接与苯环相连,官能团是酚羟基,故答案为:醇羟基、碳碳双键;酚羟基;
(2)A属于醇类,醇羟基不能电离出氢离子,所以A无酸性,不能与氢氧化钠溶液反应,B属于酚类,酚具有弱酸性,可以与氢氧化钠溶液发生酸碱中和反应,故答案为:不能;能;
(3)A结构中,与醇羟基相连的碳原子的邻碳上有氢原子,可以发生消去反应,所以对比A和B的结构可知,A转化为B发生的是消去反应,故答案为:消去反应;
(4)1molA结构中含有1mol碳碳双键,1mol碳碳双键能与1mol的溴发生加成反应,B结构中酚羟基会使邻、对位上的氢原子活化,但对位有甲基,所以只有酚羟基的邻位碳原子上的氢原子会被单质溴取代,所以1molB消耗2mol溴,故答案为:1;2。


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
【题目】常温下,2NH3(g)+NaClO(aq)=NaCl(aq)+N2H4(aq)+H2O(l)能自发进行,可用于生产N2H4。下列有关说法正确的是( )
A.该反应的ΔH>0,ΔS<0
B.每生成1molN2H4转移2mol电子
C.室温下,向0.1mol·L-1NaClO溶液中加水,溶液pH减少
D.N2H4、O2和KOH溶液组成的燃料电池,负极反应为N2H4-4e-=N2+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚被称为“21世纪的清洁燃料”。利用甲醇脱水可制得二甲醚。反应方程式如下:2CH3OH(g)≒CH3OCH3(g)+H2O(g) ΔH1
(1) 二甲醚亦可通过合成气反应制得,相关热化学方程式如下:2H2(g)+CO(g)≒CH3OH(g) ΔH2
CO(g)+H2O(g)≒CO2(g)+H2(g) ΔH3 3H2(g)+3CO(g)≒CH3OCH3(g) +CO2(g) ΔH4
则ΔH1=__________________(用含有ΔH2、ΔH3、ΔH4的关系式表示).
(2)经查阅资料,上述甲醇脱水反应平衡常数Kp的计算式为lnKp= - 2.205+(2708.6137/T) (Kp为以分压表示的平衡常数,T为热力学温度),且催化剂吸附H2O(g)的量会受压强影响,从而进步影响催化效率。
①在一定温度范围内,随温度升高,CH3OH(g)脱水转化为CH3OCH3(g)的倾向__________ (填“增大”、“不变”或“减小”),ΔH4________2ΔH2+ΔH3 (填“>”、<”或“=”)。
物质 | CH3OH | CH3OCH3 | H2O |
分压/MPa | 0.50 | 0.50 | 0.50 |
②某温度下(此时Kp=100),在密闭容器中加入一定量CH3OH,某时刻测得各组分的压如下:
此时正、逆反应速率的大小:V正____V逆(填“>”、“<”或“=”)。
③200℃时,在密闭容器中加入一定量CH3OH,反应到达平衡状态时,体系中CH3OCH3(g)的物质的量分数为__________(填序号).
A.< 1/3 B.1/3 C.1/3~1/2 D.1/2 E.> 1/2
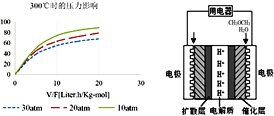
④300℃时,使CH3OH(g)以一定流速通过催化剂,V/F(按原料流率的催化剂量)、压强对甲醇转化率影响如图1所示。请简述在上述条件下,压强对甲醇转化率影响的规律,并解释变化原因__________。
(3)直接二甲醚燃料电池有望大规模商业化应用,工作原理如图2所示。
①负极的电极反应式为__________。
②现利用该电池电解CuC12溶液,当消耗2.3g二甲醚时,电解所得铜的质量为_________g(设电池的能量利用率为50%)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚维酮碘的水溶液是一种常用的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如图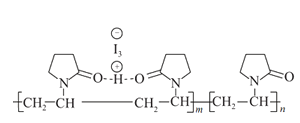 ,下列说法不正确的是( )
,下列说法不正确的是( )
A.聚维酮的单体是![]() B.聚维酮分子由(m+n)个单体聚合而成
B.聚维酮分子由(m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质D.聚维酮在一定条件下能发生水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据公安部2019年12月统计,2019年全国机动车保有量已达3.5亿。汽车尾气排放的碳氢化合物、氮氧化物及碳氧化物是许多城市大气污染的主要污染物。
I.汽油燃油车上安装三元催化转化器,可有效降低汽车尾气污染。
(1)已知:C(s)+O2(g)=CO2(g) △H1=393.5kJ·mol1
2C(s)+O2(g)=2CO(g) △H2=221.0kJ·mol1
N2(g)+O2(g)=2NO(g) △H3=+180.5kJ·mol1
CO和NO两种尾气在催化剂作用下生成N2的热化学方程式___。
(2)对于2NO(g)+2CO(g)![]() N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。
N2(g)+2CO2(g),在一定温度下,于1L的恒容密闭容器中充入0.1molNO和0.3molCO,反应开始进行。
下列能说明该反应已经达到平衡状态的是___(填字母代号)。
A.![]() 比值不变
比值不变
B.容器中混合气体的密度不变
C.v(N2)正=2v(NO)逆
D.容器中混合气体的平均摩尔质量不变
(3)使用间接电化学法可处理燃煤烟气中的NO,装置如图2所示。
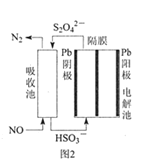
已知电解池的阴极室中溶液的pH在4~7之间,写出阴极的电极反应式__。用离子方程式表示吸收池中除去NO的原理___。
(4)T1温度时在容积为2L的恒容密闭容器中发生反应:2CO(g)+O2(g)![]() 2CO2(g) △H<0。实验测得:v正=v(CO)消耗=2v(O2)消耗=k正c2(CO)·c(O2),v逆=(CO2)消耗=k逆c2(CO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(CO)、n(O2)如表:
2CO2(g) △H<0。实验测得:v正=v(CO)消耗=2v(O2)消耗=k正c2(CO)·c(O2),v逆=(CO2)消耗=k逆c2(CO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(CO)、n(O2)如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(CO)/mol | 2 | 1.2 | 0.8 | 0.4 | 0.4 | 0.4 |
n(O2)/mol | 1.2 | 0.8 | 0.6 | 0.4 | 0.4 | 0.4 |
①T1温度时![]() =___L/mol。
=___L/mol。
②若将容器的温度改变为T2时其k正=k逆,则T2__T1(填“>”、“<”或“=")。
II.“低碳经济”备受关注,CO2的有效开发利用成为科学家研究的重要课题。在0.1MPa、Ru/TiO2催化下,将一定量的H2和CO2置于恒容密闭容器中发生反应X:CO2(g)+4H2(g) ![]() CH4(g)+2H2O(g) △H<0
CH4(g)+2H2O(g) △H<0
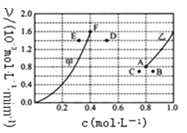
(5)为探究反应X的反应速率与浓度的关系,向恒容密闭容器中通入浓度均为1.0molL-1的H2与CO2。恒温条件下,根据相关数据绘制出反应速率与浓度关系曲线:v正~c(CO2)和v逆~c(H2O)。则与曲线v正~c(CO2)相对应的是如图___曲线。(填“甲”或“乙”);该反应达到平衡后,某一时刻降低温度,反应重新达到平衡,则此时曲线乙对应的平衡点可能为___(填字母)。
(6)温度为T时,向10L密闭容器中充入5molH2和CO2的混合气体,此时容器内压强为5P,两种气体的平衡转化率ɑ与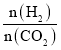 的关系如图所示:
的关系如图所示:
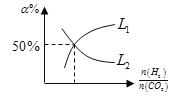
①图中CO2的平衡转化率可用表示___(L1或L2)
②该温度下,反应X的平衡常数Kp=___。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年10月9日,瑞典皇家科学院将2019年度诺贝尔化学奖授予美国JohnBGoodenough教授、M.stanleyWhittlingham教授和日本化学家AkiraYoshino,以表彰其在锂离子电池的发展方面作出的贡献。
(1)基态锂原子核外能量最高的电子所处能级的电子云轮廓图的形状为___;基态磷原子第一电离能比硫的___ (填“大”或“小”),原因是___。
(2)实室中可用KSCN或K4[Fe(CN)6]来检验Fe3+,FeCl3与KSCN溶液混合,可得到配位数为5的配合物的化学式是___;
(3)磷酸(H3PO4)和亚磷酸(H3PO3)是磷元素的两种含氧酸。PO43-的空间构型为___;亚磷酸与NaOH反应只生成NaHPO3和NaH2PO3两种盐,则H3PO3的结构式为___。
(4)磷酸分子间脱水可生成多磷酸,其某一钙盐的结构如图所示:
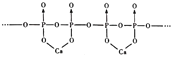
由图推知该多磷酸钙盐的通式为__(用n表示重复单元数)
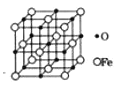
(5)氧化亚铁晶体的晶胞如图所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与O2-紧邻且等距离的Fe2+数目为__;Fe2+与O2-最短核间距为___pm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物W是一种药物的中间体,一种合成路线如图:

已知:①![]()
②![]()
请回答下列问题:
(1)A的系统命名为___。
(2)反应②的反应类型是__。
(3)反应⑥所需试剂为___。
(4)写出反应③的化学方程式为___。
(5)F中官能团的名称是___。
(6)化合物M是D的同分异构体,则符合下列条件的M共有__种(不含立体异构)。
①1molM与足量的NaHCO3溶液反应,生成二氧化碳气体22.4L(标准状态下);
②0.5molM与足量银氨溶液反应,生成108gAg固体其中核磁共振氢谱为4组峰且峰面积比为6∶2∶1∶1的结构简式为__(写出其中一种)。
(7)参照上述合成路线,以C2H5OH和![]() 为起始原料,选用必要的无机试剂合成
为起始原料,选用必要的无机试剂合成![]() ,写出合成路线__。
,写出合成路线__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种浓差电池如图所示,阴、阳离子交换膜交替放置,中间的间隔交替充以河水和海水,选择性透过Cl和Na+,在两电极板形成电势差,进而在外部产生电流。下列关于该电池的说法正确的是( )
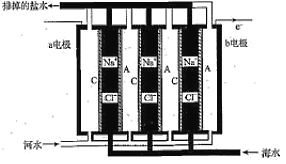
A.a电极为电池的正极,电极反应为2H++2e═H2↑
B.C为阴离子交换膜,A为阳离子交换膜
C.负极隔室的电中性溶液通过阳极表面的还原作用维持
D.该电池的缺点是离子交换膜价格昂贵,优点是电极产物有经济价值
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物H(阿戈美拉汀)是一种抗抑郁药,H的一种合成路线如下:

已知:![]()
![]()
![]() ;化合物B中含五元环结构,化合物E中含两个六元环状结构。
;化合物B中含五元环结构,化合物E中含两个六元环状结构。
回答下列问题:
(1)A的名称为_______
(2)H中含氧官能团的名称为_______
(3)B的结构简式为_______
(4)反应③的化学方程式为_______
(5)⑤的反应类型是_______
(6)M是C的一种同分异构体,M分子内除苯环外不含其他的环,能发生银镜反应和水解反应,其核磁共振氢谱有4组峰且峰面积之比为6:3:2:1。任写出三种满足上述条件的M的结构简式_______(不考虑立体异构)。
(7)结合上述合成路线,设计以2—溴环己酮( ) 和氰基乙酸(NCCH2COOH)为原料制备
) 和氰基乙酸(NCCH2COOH)为原料制备![]() 的合成路线_______(无机试剂及有机溶剂任选)
的合成路线_______(无机试剂及有机溶剂任选)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com