
| A. | 该废水中可能含有较多的Fe2+、Fe3+ | |
| B. | 此电解法缺点之一是会产生少量氯气 | |
| C. | 阳极反应式为2CN--10e-+3H2O=CO2↑+N2↑+6H+ | |
| D. | 电解法处理后的废水pH减小 |
分析 电解含CN-浓度较高的废水,阳极发生氧化反应生成氮气,阴极发生还原反应生成氢气,电解方程式为2CN-+2H++4H2O$\frac{\underline{\;电解\;}}{\;}$2CO2↑+N2↑+5H2↑,以此解答该题.
解答 解:A.铁为阴极,不能被氧化,不可能生成Fe2+、Fe3+,故A错误;
B.电解质含有氯化钠,氯离子可在阳极被氧化,则会产生少量氯气,故B正确;
C.阳极发生氧化反应,反应式为2CN--10e-+4H2O=2CO2↑+N2↑+8H+,故C错误;
D.电解方程式为2CN-+2H++4H2O$\frac{\underline{\;电解\;}}{\;}$2CO2↑+N2↑+5H2↑,则pH增大,故D错误.
故选B.
点评 本题考查电解池的工作原理,为高频考点,侧重于学生的分析能力的考查,难度不大,注意把握电极和反应类型的判断,把握电极反应,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池反应为Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O,放电时负极质量减轻 | |
| B. | 电解精炼铜时,以粗铜作阴极,纯铜作阳极 | |
| C. | CH3COONa稀溶液加水稀释后,溶液中$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$ 的值增大 | |
| D. | CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
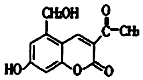 某种利胆解痉药的有效成分是亮菌甲素,其结构简式如图所示.下列关于亮菌甲素的说法中,正确的是( )
某种利胆解痉药的有效成分是亮菌甲素,其结构简式如图所示.下列关于亮菌甲素的说法中,正确的是( )| A. | 亮菌甲素的分子式为C12H12O5 | |
| B. | 1mol亮菌甲素最多能和2molNaOH反应 | |
| C. | 1mol亮菌甲素最多能和4 molH2发生加成反应 | |
| D. | 亮菌甲素在一定条件下可以与乙酸发生酯化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
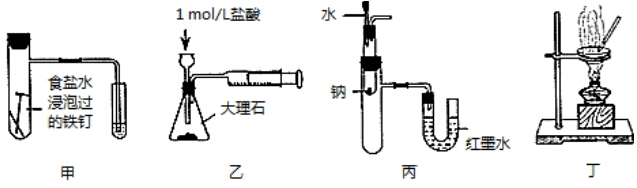
| A. | 用图甲装置验证铁发生析氢腐蚀 | |
| B. | 用图乙装置测定反应速率 | |
| C. | 用图丙装置验证Na和水反应的热效应 | |
| D. | 用图丁装置蒸干MgCl2溶液制备无水MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中和等体积、等pH的CH3COOH溶液和HCN溶液消耗NaOH的量前者小于后者 | |
| B. | 常温下,等浓度CH3COONa溶液的pH大于NaCN溶液的pH | |
| C. | 常温下,等体积、等浓度CH3COONa溶液的离子总数等于NaCN溶液的离子总数 | |
| D. | 反应CH3COOH+CN-?HCN+CH3COO-的化学平衡常数为2.8×10-5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气态氢化物的热稳定性:E>d>J | |
| B. | 原子半径:G>E>J>D | |
| C. | 最高价氧化物对应水化物的酸性:J>D>G | |
| D. | E和J组成的化合物常作食品的干燥剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.25mol Na2O2中含有的阴离子数为0.5NA | |
| B. | 等物质的量的OH-与烃基(-OH)所含电子数相等 | |
| C. | 惰性电极电解食盐水,若电路中通过NA个电子,则标况下阳极产生气体11.2L | |
| D. | 25℃时,pH=13的1.0LBa(OH)2溶液中含OH-数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
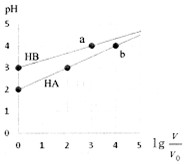 室温下,浓度均为0.1mol•L-1、体积均为V0HA、HB溶液,分别加水稀释至V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列说法正确的是( )
室温下,浓度均为0.1mol•L-1、体积均为V0HA、HB溶液,分别加水稀释至V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列说法正确的是( )| A. | HA为强酸,HB为弱酸 | |
| B. | 水的电离程度a点大于b点 | |
| C. | 当pH=2时,HA溶液中$\frac{c(HA)}{c({A}^{-})}$=9 | |
| D. | 等浓度等体积的HB与Na0H溶液充分反应后,离子浓度关系大小为:c(B-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省徐州市高二上第一次月考化学试卷(解析版) 题型:选择题
a g Mg、Al合金完全溶解在C1 mol·L-1、V1L HCl溶液中,产生b g H2。再向反应后的溶液中加入C2 mol·L-1、V2 L NaOH溶液,恰好使沉淀达到最大值,且沉淀质量为d g。下列关系错误的是 ( )
A.铝为 (24b-a)/9 mol B.C1=C2V2/V1
C.d=a+17b D.与金属反应后剩余盐酸为(C1V1-b)mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com