���
�⣺A��B��C��D��E����Ԫ�أ���λ�����ڱ���ǰ�����ڣ����ǵĺ˵�����������ӣ��Һ˵����֮��Ϊ57��Bԭ�ӵ�L��P�������2�����ӣ���ԭ�Ӻ�������Ų�Ϊ1s
22s
22p
2����BΪ̼Ԫ�أ�Eԭ�ӵ�K�������������������֮��Ϊ2��1����d�������ȫ����״̬����Eԭ�Ӻ��������=2+8+18+1=29����EΪCuԪ�أ�D��Bԭ�ӵļ۵�������ͬ�����ԭ��������֪DΪSi��C��ԭ�Ӻ���������δ�ɶԵ��ӣ�ԭ������С��Si��������Χ�����Ų�Ϊ2s
22p
3����CΪNԪ�أ���Ԫ�غ˵����֮��Ϊ57����A�ĺ˵����=57-6-7-14-29=1����AΪHԪ�أ�
��1��C��Si�ɷֱ���HԪ���γ�ֻ��һ������ԭ�ӵĹ��ۻ�����X��Y����XΪCH
4��YΪSiH
4��
CH
4������Cԭ����Hԭ��֮���γ�1�Թ��õ��Ӷԣ������ʽΪ����SiH
4��Siԭ�ӳ�4���Ҽ��������µ��Ӷԣ���Siԭ�Ӳ�ȡsp
3�ӻ���N��H�γɵij���������ΪNH
3�����ӹ���Ϊ�����Σ�
�ʴ�Ϊ��

��sp
3��������
��2��B��D�����������ֱ�ΪCO
2��SiO
2������SiO
2��ԭ�Ӿ����CO
2�Ƿ��Ӿ��壬���۵�ϸߣ�
�ʴ�Ϊ��SiO
2��SiO
2��ԭ�Ӿ����CO
2�Ƿ��Ӿ��壻
��3��ͬ������ԭ����������Ԫ�ص�һ�����ܳ��������ƣ���NԪ��2p�ܼ�Ϊ�����ȶ�״̬����NԪ�ص�һ�����ܸ���̼Ԫ�أ�Cu
2+�ĺ�������Ų�ʽΪ1s
22s
22p
63s
23p
63d
9��
�ʴ�Ϊ��N��1s
22s
22p
63s
23p
63d
9��
��4��Cu
2+��C�ij����⻯��NH
3�γɵ������ӵ����ӷ�Ӧ����ʽΪCu
2++4NH
3�T[Cu��NH
3��
4]
2+���ʴ�Ϊ��Cu
2++4NH
3�T[Cu��NH
3��
4]
2+��
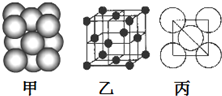
��5����ͼ��֪������Ϊ���������ѻ����Զ����ԭ�ӷ�����λ�����ĵ�ԭ����֮���������1������ԭ��Ϊ12���湲�ã�����λ��Ϊ12��
��ԭ�Ӱ뾶Ϊd����ͼ����֪�������ζԽ��߳���Ϊ4d����������ⳤΪ
��4d=2
d�����������2
d ��
3=16
d
3 �������к���ԭ����Ŀ=8��
+6��
=4��Al���ԭ������ΪM���ʾ���������=4��
g���ʾ�����ܶ�=
=
��
����Ϊ�����������ܶѻ����ռ�������Ϊ74%��
�ʴ�Ϊ��12��
��74%��

 A��B��C��D��E����Ԫ�أ���λ�����ڱ���ǰ�����ڣ����ǵĺ˵�����������ӣ��Һ˵����֮��Ϊ57��Bԭ�ӵ�L��P�������2�����ӣ�C��ԭ�Ӻ���������δ�ɶԵ��ӣ�D��Bԭ�ӵļ۵�������ͬ��Eԭ�ӵ�K�������������������֮��Ϊ2��1����d�������ȫ����״̬��
A��B��C��D��E����Ԫ�أ���λ�����ڱ���ǰ�����ڣ����ǵĺ˵�����������ӣ��Һ˵����֮��Ϊ57��Bԭ�ӵ�L��P�������2�����ӣ�C��ԭ�Ӻ���������δ�ɶԵ��ӣ�D��Bԭ�ӵļ۵�������ͬ��Eԭ�ӵ�K�������������������֮��Ϊ2��1����d�������ȫ����״̬�� ��sp3�������Σ�
��sp3��������

 �߲������Ӧ��һ��ͨϵ�д�
�߲������Ӧ��һ��ͨϵ�д�
 ��Դ�����ö�����̼�����ɼ�������������ŷţ��������»��ȼ�ϻ���Ҫ��ҵ��Ʒ��
��Դ�����ö�����̼�����ɼ�������������ŷţ��������»��ȼ�ϻ���Ҫ��ҵ��Ʒ��