
| A、氧化产物为Cl2 |
| B、若有3molH2O生成,则反应中有2mol电子转移 |
| C、微粒的还原性Cl->Co2+ |
| D、氧化剂与还原剂的物质的量之比为1:6 |


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:
| A、Fe3+、Na+、Br- |
| B、NH4+、Na+、AlO2- |
| C、Ba2+、Al3+、Cl- |
| D、K+、Mn4-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钢铁生锈与氧气、水蒸气有关,且以吸氧腐蚀为主 |
| B、氢氧化钠固体潮解、变质与水蒸气、二氧化碳有关 |
| C、浓硫酸露置于空气中浓度变小,与水蒸气有关 |
| D、钢铁在潮湿的空气中发生电化腐蚀,其正极的电极反应式为Fe-2e=Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
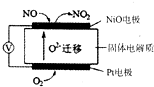 NO2是汽车尾气中的主要污染物之一.
NO2是汽车尾气中的主要污染物之一.
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.05 | n2 | 0.08 | 0.08 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 钠钾是活泼的碱金属,过氧化钠(Na2O2)、过氧化钾(K2O2)和超氧化钾(KO2) 在医院、矿井、潜水、高空飞行中用作供氧剂.某航天飞行器座舱内空气更新过程如图所示:
钠钾是活泼的碱金属,过氧化钠(Na2O2)、过氧化钾(K2O2)和超氧化钾(KO2) 在医院、矿井、潜水、高空飞行中用作供氧剂.某航天飞行器座舱内空气更新过程如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、离子半径大小关系是Xn-<Yn+ |
| B、Z一定是稀有气体元素的原子 |
| C、原子序数关系是Z>Y>X |
| D、原子半径关系是Y<X |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Y、Z、R的简单离子具有相同的电子层结构 |
| B、X、Z分别与Y均可形成A2B与A2B2型化合物,且A2B2均有较强的氧化性 |
| C、X2Y分子同存在氢键,故X2Y比X2W稳定 |
| D、由X、Y、Z形成的化合物能与X、Y、R形成的化合物发生复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、S8转化为S6、S4、S2属于物理变化 |
| B、不论哪种硫分子,完全燃烧时都生成SO2 |
| C、S8、S6、S4、S2均属于共价化合物 |
| D、把硫单质在空气中加热到750℃即得S2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com