
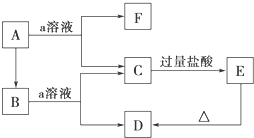
分析 A是一种固体单质,系列转化得到C,C与过量的盐酸反应得到白色沉淀E,则E为H2SiO3,C为硅酸盐,A为Si,B为SiO2,a为强碱溶液等,F为氢气、D为水,据此解答.
解答 解:A是一种固体单质,系列转化得到C,C与过量的盐酸反应得到白色沉淀E,则E为H2SiO3,C为硅酸盐,A为Si,B为SiO2,a为强碱溶液等,F为氢气、D为水.
(1)B的化学式是SiO2,目前已被用作光导纤维的主要原料,故答案为:SiO2;光导纤维;
(2)B和a溶液反应的离子方程式是:SiO2+2OH-=SiO32-+H2O,故答案为:SiO2+2OH-=SiO32-+H2O;
(3)C和过量盐酸反应的离子方程式是:SiO32-+2H+=H2SiO3↓,故答案为:SiO32-+2H+=H2SiO3↓.
点评 本题考查无机物推断,涉及Si元素单质化合物性质,C与过量盐酸反应得到白色沉淀为推断突破口,难度中等.


 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源: 题型:解答题

| 物质 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
| pKsp | 37.4 | 19.32 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaClO溶液中通入少量CO2,ClO-水解程度增大,溶液碱性增强 | |
| B. | 铁片镀锌时,铁片与外电源的正极相连 | |
| C. | 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)能自发进行,则△H<0 | |
| D. | t℃时,恒容密闭容器中反应:NO2(g)+SO2(g)?NO(g)+SO3(g),通入少量O2,$\frac{c(NO)•c(S{O}_{3})}{c(N{O}_{2})•c(S{O}_{2})}$的值及SO2转化率不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳的燃烧热大于 110.5 kJ/mol | |
| B. | ①的反应热为 221 kJ/mol | |
| C. | 稀硫酸与稀 NaOH溶液反应的中和热为-57.3kJ/mol | |
| D. | 稀醋酸与稀 NaOH溶液反应生成 1mol水,放出 57.3kJ热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下反应 |
| B | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液显紫红色 | 氧化性:Fe3+>I2 |
| C | 将可调高度的铜丝伸入到稀HNO3中 | 溶液变蓝 | Cu与稀HNO3发生置换反应 |
| D | 向AgNO3溶液中滴加过量氨水 | 溶液澄清 | Ag+与NH3?H2O能大量共存 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com