
| A. | 油脂水解可得到氨基酸和甘油 | |
| B. | 淀粉和纤维素水解最终产物都是葡萄糖 | |
| C. | 蛋白质水解的最终产物是氨基酸,某些蛋白质可用硝酸来检验 | |
| D. | 葡萄糖可用新制的氢氧化铜来检验 |
分析 A.油脂水解得到的是高级脂肪酸和甘油;
B.淀粉和纤维素都是多糖,二者水解最终产物都是葡萄糖;
C.蛋白质水解的最终产物为氨基酸,带有苯环的蛋白质与硝酸可发生颜色反应;
D.葡萄糖分子中含有醛基,能够与新制的氢氧化铜反应生成砖红色沉淀氧化亚铜.
解答 解:A.油脂为高级脂肪酸甘油酯,油脂水解得到的是高级脂肪酸和甘油,不会得到氨基酸,故A错误;
B.淀粉和纤维素都属于多糖,二者在一定条件下发生水解,最终水解产物都是葡萄糖,故B正确;
C.蛋白质能够发生水解,最终水解产物为氨基酸,带有苯环的蛋白质与硝酸可发生颜色反应,可据此检验蛋白质,故C正确;
D.葡萄糖分子中含有醛基,可用新制的氢氧化铜来检验,故D正确;
故选A.
点评 本题考查了常见有机物组成、结构与性质,题目难度不大,明确蛋白质、油脂、糖类的性质为解答关键,试题侧重基础知识的考查,有利于提高学生灵活应用基础知识的能力.


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:实验题
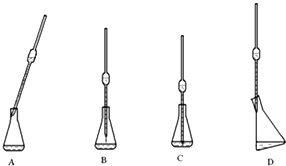 利用所学化学知识解答问题:
利用所学化学知识解答问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:6 | B. | 6:1 | C. | 1:5 | D. | 5:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
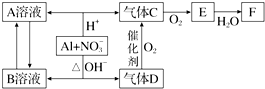
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 (R1、R2、R3为烃基或氢原子)
(R1、R2、R3为烃基或氢原子) (写结构简式).
(写结构简式).查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两者都具有丁达尔效应 | |
| B. | 分散质的粒子直径均在1~100nm之间 | |
| C. | 加烧碱溶液都会沉淀 | |
| D. | 前者是混合物,后者是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用湿润的pH试纸测定某待测液的pH,数值一定偏大 | |
| B. | 25℃时,pH=2的一元酸溶液与pH=12的一元碱溶液等体积混合,所得溶液pH=7 | |
| C. | 在(NH4)2Fe(SO4)2溶液中,c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-) | |
| D. | pH相同的NaOH和CH3COONa两种稀溶液,若稀释后,pH仍相同,则稀释的倍数相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com