
【题目】某学生为探究钠与二氧化碳的反应,利用如图装置进行实验。
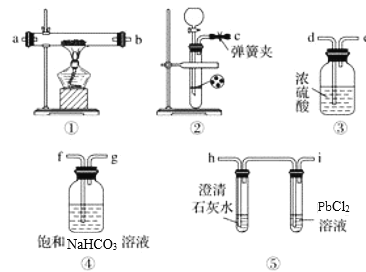
已知PdCl2能被一氧化碳还原得到黑色的Pd.请回答下列问题:
(1)请将如图各装置连接完整:c接f,_____接_____,_____接_____,_____接_____。
(2)若用稀盐酸与碳酸钙反应制备二氧化碳,在加稀盐酸时,发现碳酸钙与稀盐酸不能接触,而稀盐酸又不够了,为使反应能顺利进行,可向长颈漏斗中加入的试剂是_____(填字母)。
A.硝酸钠溶液 B.四氯化碳 C.苯 D.稀硝酸
(3)检查装置气密性并装好药品后,点燃酒精灯之前应进行的操作是打开弹簧夹,让二氧化碳充满整个装置,当观察到_____时,再点燃酒精灯。此步操作的目的是_____________________。
(4)反应过程中二氧化碳足量,假如装置⑤PdCl2溶液中观察到有黑色沉淀,装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体。写出钠与二氧化碳反应的化学方程式_______________________________。
【答案】g d e a(b) b(a) h ABD 装置⑤中澄清石灰水变浑浊 排尽装置中的空气,以免空气中O2、H2O干扰实验 2Na+2CO2![]() Na2CO3+CO
Na2CO3+CO
【解析】
先利用稀盐酸和石灰石在装置②中反应制取二氧化碳,生成的二氧化碳中会混有HCl气体,可以用饱和碳酸氢钠溶液除去,之后用浓硫酸进行干燥,然后通入装置①中与Na进行反应,然后通过装置⑤对产物进行检验。
(1)根据分析可知c接f,g接d,e接a(b),b(a)接h;
(2)装置②中碳酸钙放置在多孔板上方,需要试管中液体淹没碳酸钙进行反应,加入硝酸钠溶液、稀硝酸都可以使溶液体积增大淹没碳酸钙;四氯化碳虽然与水不互溶,但密度比水大,所以加入后会在下层,使无机层液面上升淹没碳酸钙,而苯的密度比水小,会浮在稀盐酸上方,无法使稀盐酸淹没碳酸钙,所以选ABD;
(3)装置⑤中澄清石灰水变浑浊时,可以说明二氧化碳充满了整个装置;该操作可以排尽装置中的空气,以免空气中O2、H2O干扰实验;
(4)装置⑤PdCl2溶液中观察到有黑色沉淀,说明有CO生成;装置①中固体成分只有一种,且向固体中加入稀盐酸产生能使澄清石灰水变浑浊的气体,根据元素守恒可知该固体应为碳酸钠,所以化学方程式为2Na+2CO2![]() Na2CO3+CO。
Na2CO3+CO。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】HI常用作有机反应中的还原剂,受热会发生分解反应。已知443℃时:2HI(g)![]() H2(g)+I2(g) △H=+12.5kJ·mol-1向1L密闭容器中充入1mol HI,443℃时,体系中c(HI)与反应时间t的关系如图所示。下列说法中,正确的是( )
H2(g)+I2(g) △H=+12.5kJ·mol-1向1L密闭容器中充入1mol HI,443℃时,体系中c(HI)与反应时间t的关系如图所示。下列说法中,正确的是( )

A.0~20min内的平均反应速率可表示为v(H2)=0.0045mol·L-1·min-1
B.升高温度,再次平衡时,c(HI)>0.78mol·L-1
C.该反应的化学平衡常数计算式为![]()
D.反应进行40 min时,体系吸收的热量约为0.94kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据如图有关图象,说法正确的是( )
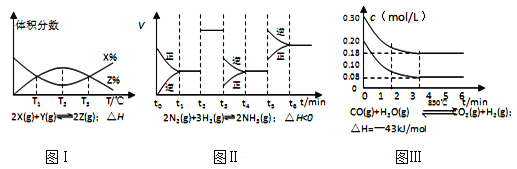
A. 由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的△H<0
B. 由图Ⅱ知,反应在t6时刻,NH3体积分数最大
C. 由图Ⅱ知,t3时采取降低反应体系温度的措施
D. 图Ⅲ表示在10L容器、850℃时的反应,由图知,到4min时,反应放出51.6kJ的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学对铜与浓硫酸反应产生的黑色沉淀进行探究,实验步骤如下:
Ⅰ.将光亮铜丝插入浓硫酸,加热;
Ⅱ.待产生黑色沉淀和气体时,抽出铜丝,停止加热;
Ⅲ.冷却后,从反应后的混合物中分离出黑色沉淀,洗净、干燥备用。
查阅文献:检验微量Cu2+的方法是:向试液中滴加K4[Fe(CN)6] 溶液,若产生红
褐色沉淀,证明有Cu2+。
(1)该同学假设黑色沉淀是CuO。检验过程如下:
①将CuO放入稀硫酸中,一段时间后,再滴加K4[Fe(CN)6] 溶液,产生红褐色沉淀。
②将黑色沉淀放入稀硫酸中,一段时间后,再滴加K4[Fe(CN)6] 溶液,未见红褐色沉淀。由该检验过程所得结论是_______________。
(2)再次假设,黑色沉淀是铜的硫化物。实验如下:
实验装置 | 现象 |
| 1. A试管中黑色沉淀逐渐溶解 |
①现象2说明黑色沉淀具有______性。
②能确认黑色沉淀中含有S元素的现象是_________,相应的离子方程式是_____________。
③为确认黑色沉淀是“铜的硫化物”,还需进行的实验操作是___________________。
(3)以上实验说明,黑色沉淀中存在铜的硫化物。进一步实验后证明黑色沉淀是CuS与Cu2S的混合物。将黑色沉淀放入浓硫酸中加热一段时间后,沉淀溶解,其中CuS溶解的化学方程式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于硝酸的说法中正确的是( )
A.硝酸电离出的H+,能被Zn还原成H2
B.常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体
C.向装有Fe(NO3)2溶液的试管中加入稀H2SO4,可在管口观察到红棕色气体
D.过量的Fe粉中加入稀HNO3,充分反应后,滴入KSCN溶液,溶液呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】活性炭可处理大气污染物NO,反应原理:C(s)+2NO(g)![]() N2(g)+CO2(g)。T℃时,在2L密闭容器中加入0.100molNO和2.030mol活性炭(无杂质),平衡时活性炭物质的量是2.000mol。下列说法不合理的是
N2(g)+CO2(g)。T℃时,在2L密闭容器中加入0.100molNO和2.030mol活性炭(无杂质),平衡时活性炭物质的量是2.000mol。下列说法不合理的是
A.该温度下的平衡常数是:K=![]()
B.达到平衡时,NO的转化率是60%
C.3min末达到平衡,则v(NO)=0.01mol/(L·min)
D.若平衡时再加入0.100molNO,则达到新平衡时NO的转化率比原平衡时低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,HA的电离常数Ka=1×10-6,向20 mL浓度为0.01 mol·L-1的HA溶液中逐滴加入0.01mol·L-1的NaOH溶液,溶液的pH与加入NaOH溶液的体积之间的关系如图所示,下列说法正确的是( )

A.a点对应溶液的pH约为4,且溶液中只存在HA的电离平衡
B.b点对应溶液中:c(Na+)>c(A-)>c(HA)>c(H+)>c(OH-)
C.d点对应溶液中:c(OH-)-c(H+)=c(A-)
D.a、b、c、d四点对应的溶液中水的电离程度:a<b<c<d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行实验,下列对实验现象的解释不合理的是

①中试剂 | ①中现象 | 解释 | |
A | 品红溶液 | 溶液褪色 | SO2具有漂白性 |
B | Na2SiO3溶液 | 产生胶状沉淀 | 酸性:H2SO3>H2SiO3 |
C | 酸性KMnO4溶液 | 紫色褪去 | SO2具有还原性 |
D | 酸性Ba(NO3)2溶液 | 生成白色沉淀 | SO32-与Ba2+生成BaSO3沉淀 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com