
| 实验序号 | 实验内容 | 实验结果 |
| a | 加AgNO3溶液 | 有白色沉淀生成 |
| b | 加足量NaOH溶液并加热 | 收集到气体1.12L(已折算成标准 状况下的体积) |
| c | 加足量BaCl2溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.27g,第二次 称量读数为2.33g |
分析 a中加入AgNO3溶液有沉淀产生,说明溶液中可能存在Cl-、CO32-、SO42-;
b中1.12L为氨气,氨气的物质的量为0.05mol,溶液中一定含有NH4+,并且物质的量为0.05mol;
c中2.33g为硫酸钡,硫酸钡的物质的量为0.01mol;6.27g为硫酸钡和碳酸钡,碳酸钡的质量为6.27g-2.33g=3.94g,物质的量为0.02mol;溶液中一定存SO42-、CO32-,根据离子共存可知,一定不存在Cu2+、Ba2+、Ca2+,结合电荷守恒解答该题.
解答 解:a中加入AgNO3溶液有沉淀产生,说明溶液中可能存在Cl-、CO32-、SO42-;
b中1.12L为氨气,氨气的物质的量为0.05mol,溶液中一定含有NH4+,并且物质的量为0.05mol;
c中2.33g为硫酸钡,硫酸钡的物质的量为0.01mol;6.27g为硫酸钡和碳酸钡,碳酸钡的质量为6.27g-2.33g=3.94g,物质的量为0.02mol;溶液中一定存SO42-、CO32-,根据离子共存可知,一定不存在Cu2+、Ba2+、Ca2+,
(1)由上述分析可知,一定不存在Mg2+、Cu2+、Ba2+,故答案为:Mg2+、Cu2+、Ba2+;
(2)一定存在的阴离子为SO42-、CO32-,故答案为:SO42-、CO32-;
(3)实验b发生反应的离子方程式为NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3+H2O,故答案为:NH4++OH- $\frac{\underline{\;\;△\;\;}}{\;}$NH3+H2O;
(4)由从题中可确定:NH4+ 0.05mol,SO42- 0.01mol,CO32- 0.02mol,根据离子的电荷守恒可知一定有K+,故答案为:是;NH4+ 0.05mol,SO42- 0.01mol,CO32- 0.02mol.
点评 本题考查无机物的推断,把握常见离子的检验方法、离子反应及电荷守恒为解答的关键,侧重分析与推断、应用能力的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题

| A. | 丹参素的分子式为C9H9O5 | |
| B. | 丹参素能发生缩聚、消去、氧化反应 | |
| C. | 1 mol丹参素最多可以和4 mol H2发生加成反应 | |
| D. | 丹参素分子中含有手性碳原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | -824.39 kJ•mol-1 | B. | +627.6 kJ•mol-1 | ||
| C. | -744.7 kJ•mol-1 | D. | -169.4 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 丙烷、丁烷、正戊烷的沸点依次降低 | |
| B. | 乙二醇、丙氨酸均可发生缩聚反应 | |
| C. | 蔗糖和麦芽糖水解的最终产物都是葡萄糖 | |
| D. | 饱和(NH4)2SO4溶液可导致蛋清液变性凝固 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气的燃烧热△H=-241.8KJ/mol | |
| B. | 相同条件下,充分燃烧1molH2(g)与1molS(g)的混合物比充分燃烧1mol H2S(g)放热多20.1kJ | |
| C. | 由①②知,水的热稳定性小于硫化氢 | |
| D. | ②中生成固态硫,△H将增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,向100mL 0.l mol.L-lHCl的溶液p 中逐滴加入0.2mol.L-lMOH溶液的过程中,其pH变化如图所示(溶液体积变化忽略不计).下列说法中正确的是( )
常温下,向100mL 0.l mol.L-lHCl的溶液p 中逐滴加入0.2mol.L-lMOH溶液的过程中,其pH变化如图所示(溶液体积变化忽略不计).下列说法中正确的是( )| A. | MOH为一元强碱 | |
| B. | N点水的电离程度小于K点水的电离程度 | |
| C. | 在K点,c(M+)>c(Cl-)>c(OH-)>c(H+) | |
| D. | K点对应的溶液中,有c( MOH)+c( M+)=0.2 mol.L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
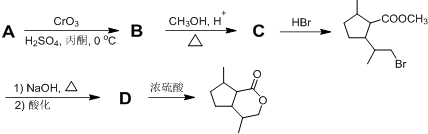
 ,B含有的官能团的名称是羧基、碳碳双键.
,B含有的官能团的名称是羧基、碳碳双键. .
. ,若该高聚物平均相对分子质量约为20000,则其平均聚合度约为c(填标号).
,若该高聚物平均相对分子质量约为20000,则其平均聚合度约为c(填标号). ,其分子中最多有8个碳原子在同一平面上.
,其分子中最多有8个碳原子在同一平面上.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )为原料合成某重要的有机物X、Y,路线如下(部分反应条件略):
)为原料合成某重要的有机物X、Y,路线如下(部分反应条件略):



 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com