

 ��F���еĹ������������Ȼ����ǻ���
��F���еĹ������������Ȼ����ǻ��� ��
�� ��
�� ��
������ A���巢���ӳɷ�Ӧ����B����B�Ľṹ��ʽ��֪AΪCH3CH2C��CH3��=CH2��B����ˮ�ⷴӦ����CΪ ��C����������Ӧ����D����D�ķ���ʽ��֪C���ǻ�����Ϊ�Ȼ�����DΪ
��C����������Ӧ����D����D�ķ���ʽ��֪C���ǻ�����Ϊ�Ȼ�����DΪ ���Ƚ�D��E�ķ���ʽ��֪��D��ȥ1����ˮ����E��Ӧ��D������ȥ��Ӧ����E����EΪ
���Ƚ�D��E�ķ���ʽ��֪��D��ȥ1����ˮ����E��Ӧ��D������ȥ��Ӧ����E����EΪ ��
�� ��
�� ����������ˮ��Һ�����������·���ˮ�ⷴӦ���ữ�õ�F����FΪ
����������ˮ��Һ�����������·���ˮ�ⷴӦ���ữ�õ�F����FΪ ��E��F����������Ӧ�õ�G�������G�ķ���ʽ��֪GΪ
��E��F����������Ӧ�õ�G�������G�ķ���ʽ��֪GΪ ���Դ������
���Դ������
��� �⣺��1��AΪCH3CH2C��CH3��=CH2������Ϊ2-��-1-��ϩ��CΪ �������к���6�ֻ�ѧ������ͬ��Hԭ�ӣ���˴Ź�����������6�����շ壮D�Ľṹ��ʽΪ
�������к���6�ֻ�ѧ������ͬ��Hԭ�ӣ���˴Ź�����������6�����շ壮D�Ľṹ��ʽΪ ��FΪ
��FΪ �����еĹ����������ǣ��Ȼ����ǻ���
�����еĹ����������ǣ��Ȼ����ǻ���
�ʴ�Ϊ��2-��-1-��ϩ��6�� ���Ȼ����ǻ���
���Ȼ����ǻ���
��2����Ӧ�����ڼӳɷ�Ӧ����Ӧ��������ȥ��Ӧ��
�ʴ�Ϊ���ӳɷ�Ӧ����ȥ��Ӧ��
��3����Ӧ�ݵĻ�ѧ����ʽΪ ��
��
�ʴ�Ϊ�� ����
����
��4����Ӧ�Ļ�ѧ����ʽΪ ��
�� ��
��
�ʴ�Ϊ�� ��
�� ��
��
��5��F�� ���ж���ͬ���칹�壬������������������ͬ���칹�壺����FeC13��Һ������ɫ��Ӧ������-OH���ڱ��������������ȡ�������ұ����ϵ�һ±����ֻ�����֣�������ֻ��2��H�����ܷ���������Ӧ����-CHO����1mol���л������������Ʒ�Ӧ�����ɱ�״����22.4L�����壬��2��-OH��������������
���ж���ͬ���칹�壬������������������ͬ���칹�壺����FeC13��Һ������ɫ��Ӧ������-OH���ڱ��������������ȡ�������ұ����ϵ�һ±����ֻ�����֣�������ֻ��2��H�����ܷ���������Ӧ����-CHO����1mol���л������������Ʒ�Ӧ�����ɱ�״����22.4L�����壬��2��-OH��������������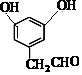 ��
�� ��
�� ����3�֣�
����3�֣�
�ʴ�Ϊ��3��
���� ���⿼���л���ĺϳɣ�Ϊ��Ƶ���㣬���պϳ������й����ŵı仯���л���ӦΪ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע���л������ʵ�Ӧ�ã���Ŀ�ѶȲ���


 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д� �ۺ��Բ�ϵ�д�
�ۺ��Բ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
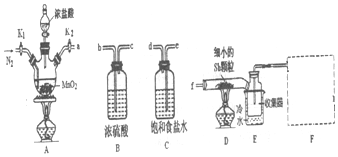
 ����ͼ��ʾװ�ü�����������ʱ�����ܴﵽĿ���ǣ�������
����ͼ��ʾװ�ü�����������ʱ�����ܴﵽĿ���ǣ�������| ѡ�� | ���ɵ����� | �Լ�X | �Լ�Y |
| A | ��ʯ��ˮ��Ӧ��ȡ����Ȳ | CuSO4��Һ | ��ˮ |
| B | ľ̿��ŨH2SO4���ȵõ��Ķ�����̼ | ����NaHCO3��Һ | ����ʯ��ˮ |
| C | CH3CH2Br��NaOH����Һ���ȵ� ������ϩ | ˮ | KMnO4 ������Һ |
| D | C2H5OH��ŨH2SO4������170����ȡ����ϩ | NaOH��Һ | ��ˮ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 �����£���10mL0.1mol/L��ijһԪ��HR��Һ����μ���0.1mol/L��ˮ��������ҺpH�����������仯��ͼ�����з�������ȷ���ǣ�������
�����£���10mL0.1mol/L��ijһԪ��HR��Һ����μ���0.1mol/L��ˮ��������ҺpH�����������仯��ͼ�����з�������ȷ���ǣ�������| A�� | a��b�㵼��������ǿ˵��HRΪ���� | |
| B�� | a��b����ʾ��Һ��ˮ�ĵ���̶Ȳ���ͬ | |
| C�� | bǡ����ȫ�кͣ�pH=7˵��NH4Rû��ˮ�� | |
| D�� | c ����Һ����c��NH4+����c��R-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ����Ļ�ѧʽ | CH3COOH | HCN | H2S |
| ���볣�� | 1.8��10-5 | 4.9��10-10 | K1=9.1��10-8 K2=1.1��10-12 |
| A�� | �����ʵ���Ũ�ȵĸ���Һ pH ��ϵΪ��pH��Na2S����pH��NaCN����pH��NaHS����pH��CH3COONa�� | |
| B�� | �� 0.1mol/L �� NaOH ��Һ�ζ� pH ֵ��ȵ�CH3COOH�� HCN ��Һ��CH3COOH���ĵ�NaOH��Һ��� ���� | |
| C�� | NaHS ��Na2S �Ļ����Һ�У�һ������c��Na+��+c��H+��=c��OH-��+c��HS-��+2c��S2-��+c��H2S�� | |
| D�� | ijŨ�ȵ�NaCN��Һ�� pH=d����������ˮ�������c��OH-��=10-4mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ƽ��ʱ�������е�ѹǿ����ȣ�����������ѹǿ֮��Ϊ8��5 | |
| B�� | ��ƽ��ʱ���ס�����������A�����ʵ�����ȣ���x=2 | |
| C�� | ��ƽ��ʱ���ס�����������A�����ʵ�������ȣ���x=3 | |
| D�� | ��ƽ��ʱ���ס�����������A�����ʵ�����ȣ���Ϊ����ͬ�����Ϊ�ҵ���ʼ���ʣ��ﵽƽ���C�������������Ϊ0.2����Ӧ���淴Ӧ����ʼ����D����ʼ���ʵ���Ӧ�����������n��D����$\frac{4}{3}$ mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | þԭ����1s22s22p63s2��1s22s22p63p2ʱ��ԭ���ͷ��������ɻ�̬ת���ɼ���̬ | |
| B�� | 24Crԭ�ӵĵ����Ų�ʽ��1s22s22p63s23p63d44s2 | |
| C�� | ��ij��̬ԭ�ӵ���Χ�����Ų�Ϊ4d25s2�����ǵ�������IVB��Ԫ�� | |
| D�� | M��ȫ������N��Ϊ4s1��ԭ�Ӻ�λ�ڵ������ڵڢ�A���ԭ����ͬһ��Ԫ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����N�����ף�P�����飨As���ȶ��Ǣ�A���Ԫ�أ�����Ԫ�صĻ��������о�����������������Ҫ��;���ش��������⣺
����N�����ף�P�����飨As���ȶ��Ǣ�A���Ԫ�أ�����Ԫ�صĻ��������о�����������������Ҫ��;���ش��������⣺ ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com