
| A.0.005 mol·L-1的H2SO4溶液,pH=2 |
| B.0.001 mol·L-1的NaOH溶液,pH=11 |
| C.0.005 mol·L-1的H2SO4溶液与0.01 mol·L-1的NaOH溶液等体积混合,混合溶液的pH为6,溶液显酸性 |
| D.完全中和pH=3的H2SO4溶液50 mL,需要pH=11的NaOH溶液50 mL |
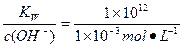 =1×10-9 mol·L-1,pH=-lg(1×10-9)=9。
=1×10-9 mol·L-1,pH=-lg(1×10-9)=9。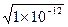 =1×10-6 mol·L-1,pH=6。虽然pH=6,但溶液不是酸性。问题的关键是c(H+)=c(OH-),溶液应该是显中性。
=1×10-6 mol·L-1,pH=6。虽然pH=6,但溶液不是酸性。问题的关键是c(H+)=c(OH-),溶液应该是显中性。

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案科目:高中化学 来源:不详 题型:填空题
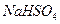 在水中的电离方程式为
在水中的电离方程式为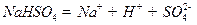 。在
。在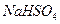 溶液
溶液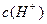 __________
__________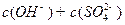 (填“>”“=”或“<”,1分)。
(填“>”“=”或“<”,1分)。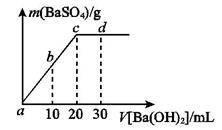
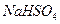 溶液中逐滴加入等物质的量浓度的
溶液中逐滴加入等物质的量浓度的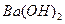 溶液,生产沉淀的量与加入氢氧化钡溶液的体积关系如图所示。a、b、c、d分别表示实验时不同阶段的溶液。其中b点表示溶液呈_________(填“酸性”“中性”或“碱性”,1分),c点所示的离子方程式为______________________________________________________(2分)。
溶液,生产沉淀的量与加入氢氧化钡溶液的体积关系如图所示。a、b、c、d分别表示实验时不同阶段的溶液。其中b点表示溶液呈_________(填“酸性”“中性”或“碱性”,1分),c点所示的离子方程式为______________________________________________________(2分)。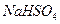 晶体加入到pH=6的蒸馏水中,保持温度不变,测得溶液的pH为2。T℃将__________25℃(填“高于”或“低于”,1分),K
晶体加入到pH=6的蒸馏水中,保持温度不变,测得溶液的pH为2。T℃将__________25℃(填“高于”或“低于”,1分),K 为__________(1分),在该溶液中由水电离出的
为__________(1分),在该溶液中由水电离出的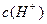 为__________mol·L-1(1分)。T℃时,将pH=11的NaOH溶液V1L与pH=1的
为__________mol·L-1(1分)。T℃时,将pH=11的NaOH溶液V1L与pH=1的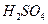 溶液V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1: V2 =____________(2分),此溶液中各种离子的浓度由大到小的排列顺序为________________________________________________(2分)。
溶液V2L混合(设混合后溶液的体积为原两溶液体积之和),所得混合溶液的pH=2,则V1: V2 =____________(2分),此溶液中各种离子的浓度由大到小的排列顺序为________________________________________________(2分)。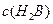 、②
、②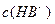 、③
、③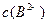 由大到小的顺序为_______________(2分)。
由大到小的顺序为_______________(2分)。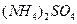 溶液、②
溶液、②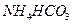 溶液、③
溶液、③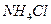 溶液中,
溶液中,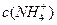 由大到小的排列顺序为_______________________(2分)。
由大到小的排列顺序为_______________________(2分)。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
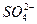 、
、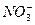 、OH-中的四种。若各自单独排放会造成较大污染,如果混合后再排放,则会大大降低污染程度。现测得甲车间排放的污水呈碱性。则
、OH-中的四种。若各自单独排放会造成较大污染,如果混合后再排放,则会大大降低污染程度。现测得甲车间排放的污水呈碱性。则查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Q1=Q2=Q3 | B.Q2>Q1>Q3 | C.Q2>Q3>Q1 | D.Q2=Q3>Q1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.5 | B.1.7 | C.2 | D.13.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.13 | B.14 |
| C.15 | D.无法确定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.自来水 | B.0.5mol/L盐酸 |
| C.0.5mol/L醋酸 | D.0.5mol/L氯化铵 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.Na+、H+、NO 、SO 、SO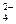 | B.Al3+、Na+、HCO 、Cl- 、Cl- |
C.H+、Cl-、SO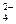 、NO 、NO | D.CO 、NO 、NO 、Cl-、K+ 、Cl-、K+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com