
”¾ĢāÄæ”æČÜŅŗÖŠ“ęŌŚÓŠĪåÖÖĄė×Ó£¬ĘäÖŠø÷Ąė×ÓøöŹż±ČCl£”ĆSO42£”ĆFe3+”ĆK+”ĆM=2”Ć3”Ć1”Ć3”Ć1£¬ŌņMĪŖ£Ø £©
A£®CO32£ B£®Mg2+ C£®Na+ D£®Ba2+
”¾“š°ø”æB
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗøł¾Żø÷Ąė×ÓøöŹż±ČCl£”ĆSO42£”ĆFe3+”ĆK+”ĆM=2£ŗ3£ŗ1£ŗ3£ŗ1£¬ÉčĀČĄė×ÓøöŹżĪŖ2n£¬ŌņŅŃÖŖµÄŅõĄė×ÓĖł“ųøŗµēŗÉ×ÜŹżĪŖ2n+3n”Į2=8n£¬ŃōĄė×ÓĖł“ųÕżµēŗÉ×ÜŹżĪŖn”Į3+3n”Į1=6n£¬ŃōĄė×ÓĖł“ųµēŗÉŹżŠ”ÓŚŅõĄė×ÓĖł“ųµēŗÉŹż£¬ŌņMĄė×ÓĪŖŃōĄė×Ó£¬ĒŅŠč“ų2øöµ„Ī»ÕżµēŗÉ£®ŅņČÜŅŗÖŠÓŠĮņĖįøłĄė×Ó£¬±µĄė×ÓÓėĮņĖįøłĄė×Ó»į½įŗĻ³ÉĮņĖį±µ³Įµķ£¬±µĄė×Ó²»ŗĻĢāŅā£¬“š°øŃ”B”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµÉĻÓĆŗ¬ĆĢ·ĻĮĻ(Ö÷ŅŖ³É·ÖMnO2£¬ŗ¬ÓŠÉŁĮæFe2O3”¢Al2O3”¢CuO”¢CaOµČ)ÓėŃĢĘųĶŃĮņ½ųŠŠĮŖŗĻ“¦Ąķ²¢ÖʱøMnSO4µÄĮ÷³ĢČēĻĀ£ŗ

ŅŃÖŖ£ŗ25”ꏱ£¬²æ·ÖĒāŃõ»ÆĪļµÄČܶȻż³£Źż(Ksp)ČēĻĀ±ķĖłŹ¾”£
ĒāŃõ»ÆĪļ | Al(OH)3 | Fe(OH)3 | Cu(OH)2 | Mn(OH)2 |
Ksp | 1.0”Į10-33 | 4.0”Į10-38 | 2.0”Į10-20 | 4.0”Į10-14 |
Ēė»Ų“š£ŗ
(1)³Įµķ1µÄ»ÆѧŹ½ĪŖ__________________”£
(2)(NH4)2SµÄµē×ÓŹ½ĪŖ________________£»”°¾»»Æ”±Ź±£¬¼ÓČė(NH4)2SµÄ×÷ÓĆĪŖ___________________”£
(3)”°Ėį»Æ”¢»¹Ō”±ÖŠ£¬·¢ÉśµÄĖłÓŠŃõ»Æ»¹Ō·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ__________________”£
(4)ŅŃÖŖ£ŗĀĖŅŗ3ÖŠ³żMnSO4Ķā£¬»¹ŗ¬ÓŠÉŁĮæ(NH4)2SO4”£(NH4)2SO4”¢MnSO4µÄČܽā¶ČĒśĻßČēĻĀĶ¼ĖłŹ¾”£
¾Ż“ĖÅŠ¶Ļ£¬²Ł×÷”°I”±Ó¦ĪŖÕō·¢ÅØĖõ”¢____________”¢Ļ“µÓ”¢øÉŌļ”£

(5)¹¤ŅµÉĻæÉÓƵē½āĖįŠŌMnSO4ČÜŅŗµÄ·½·ØÖʱøMnO2£¬ĘäŃō¼«·“Ó¦Ź½ĪŖ________________”£
(6)25.35 g MnSO4”¤H2OѳʷŹÜČČ·Ö½ā¹ż³ĢµÄČČÖŲĒśĻß(ѳʷ֏ĮæĖęĪĀ¶Č±ä»ÆµÄĒśĻß)ČēĻĀĶ¼ĖłŹ¾”£
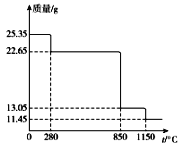
¢Ł300”ꏱ£¬ĖłµĆ¹ĢĢåµÄ»ÆѧŹ½ĪŖ______________________”£
¢Ś1150”ꏱ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ___________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ25”ꏱ£¬Ļņ20mL0.1 mol”¤L-1H2R(¶žŌŖČõĖį)ČÜŅŗÖŠµĪ¼Ó0.1 mol”¤L-1NaOHČÜŅŗ,ČÜŅŗPHÓė¼ÓČėNaOHČÜŅŗĢå»żµÄ¹ŲĻµČēĶ¼ĖłŹ¾”£ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ

A. aµćĖłŹ¾ČÜŅŗÖŠ: c(H2R) + c (HR-) +c (R2-)£½0.1 mol”¤L-1
B. bµćĖłµĆČÜŅŗÖŠ: c (H2R) + c (H+)£½ c (HR-) + c (OH-)
C. cµćĖłµĆČÜŅŗÖŠ: c (HR-)£½ c (R2-)
D. a”¢b”¢c”¢dÖŠ,dµćĖłŹ¾ČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶Č×ī“ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗ£Ė®ÖŠŗ¬ÓŠ“óĮæC1-”¢Na+¼°ÉŁĮæSO42-”¢Ca2+”¢Mg2+£¬ÓƵēÉųĪö·Ø¶ŌøĆŗ£Ė®ŃłĘ·½ųŠŠµ»Æ“¦Ąķ£¬ČēĶ¼ĖłŹ¾”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
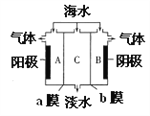
A. aĤŹĒŅõĄė×Ó½»»»Ä¤
B. A¼«ŹŅ²śÉśµÄĘųĢåæÉŹ¹ŹŖČóµÄKIµķ·ŪŹŌÖ½±äĄ¶
C. B¼«ŹŅ²śÉśĘųÅŻ²¢°éÓŠÉŁĮæ³ĮµķÉś³É
D. µ»Æ¹¤×÷Ķź³ÉŗóA”¢B”¢CČżŹŅÖŠpH“óŠ”ĪŖpH(B)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ĖłŹ¾£¬a”¢b”¢c¾łĪŖ·Ē½šŹōµ„ÖŹ£¬d”¢e¾łĪŖŗ¬ÓŠ10øöµē×ӵĹ²¼Ū»ÆŗĻĪļ£¬ĒŅ·Ö×ÓÖŠĖłŗ¬Ō×ÓøöŹż£ŗd>e£¬fĪŖĄė×Ó»ÆŗĻĪļ”£ŌņĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ

A£®³£ĪĀĻĀ£¬µ„ÖŹa³ŹĘųĢ¬ B£®µ„ÖŹc¾ßÓŠĒæŃõ»ÆŠŌ
C£®ĪČ¶ØŠŌ£ŗd£¾e D£®fŹÜČČŅ×·Ö½āĪŖdŗĶe
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ2.4g MgÓė100mLĻ”ĮņĖįĶźČ«·“Ó¦£¬·“Ó¦Ē°ŗóČÜŅŗĢå»ż±ä»ÆŗöĀŌ²»¼Ę£®
Ēó£ŗ£Ø1£©²śÉśµÄĘųĢåŌŚ±ź×¼×“æöĻĀµÄĢå»ż£®
£Ø2£©·“Ó¦ĶźČ«ŗó£¬ĖłµĆČÜŅŗÖŠĆ¾Ąė×ÓµÄĪļÖŹµÄĮæÅØ¶Č£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĖ«øōĤµē½ā³Ų£ØĮ½µē¼«¾łĪŖ¶čŠŌµē¼«£©µÄ½į¹¹Ź¾Ņā¼ņĶ¼ČēĶ¼ĖłŹ¾£¬ĄūÓĆøĆ×°ÖĆæÉŅŌµē½āĮņĖįÄĘČÜŅŗŅŌÖĘČ”ĮņĖįŗĶĒāŃõ»ÆÄĘ£¬²¢µĆµ½ĒāĘųŗĶŃõĘų”£¶ŌøĆ×°ÖĆ¼°ĘäŌĄķÅŠ¶Ļ“ķĪóµÄŹĒ

A. Čēµē¼«²ÄĮĻ¾łøÄĪŖĶ°å£¬µē½ā³ŲµÄ×Ü·“Ó¦·½³ĢŹ½²»±ä
B. ĻņAČÜŅŗÖŠµĪ¼ÓŹÆČļŹŌŅŗĻŌŗģÉ«
C. cøōĤĪŖŅõĄė×Ó½»»»Ä¤”¢døōĤĪŖŃōĄė×Ó½»»»Ä¤
D. ĻąĶ¬Ģõ¼žĻĀ£¬cøōĤø½½üµē¼«²śÉśµÄaĘųĢåÓėdøōĤø½½üµē¼«²śÉśµÄbĘųĢåĢå»ż±ČĪŖ1£ŗ2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚ³£ĪĀ³£Ń¹ĻĀ£¬Č”ĻĀĮŠĖÄÖÖĘųĢ¬Ģžø÷1g£¬·Ö±šŌŚŃõĘųÖŠĶźČ«Č¼ÉÕ£¬ĻūŗÄŃõĘų×ī¶ąµÄŹĒ£Ø£©
A.¼×ĶéB.ŅŅĶéC.ŅŅĻ©D.±ūĶé
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ[2017Ģģ½ņ]øł¾ŻŌŖĖŲÖÜĘŚ±ķŗĶŌŖĖŲÖÜĘŚĀÉ£¬ÅŠ¶ĻĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ

A£®ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗH2O£¾NH3£¾SiH4
B£®ĒāŌŖĖŲÓėĘäĖūŌŖĖŲæÉŠĪ³É¹²¼Ū»ÆŗĻĪļ»ņĄė×Ó»ÆŗĻĪļ
C£®Ķ¼1ĖłŹ¾ŹµŃéæÉÖ¤Ć÷ŌŖĖŲµÄ·Ē½šŹōŠŌ£ŗCl£¾C£¾Si
D£®ÓĆÖŠĪÄ”°![]() ”±£Øؤo£©ĆüĆūµÄµŚ118ŗÅŌŖĖŲŌŚÖÜĘŚ±ķÖŠĪ»ÓŚµŚĘßÖÜĘŚ0×å
”±£Øؤo£©ĆüĆūµÄµŚ118ŗÅŌŖĖŲŌŚÖÜĘŚ±ķÖŠĪ»ÓŚµŚĘßÖÜĘŚ0×å
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com