
”¾ĢāÄæ”æČ”100mL 18.3molL©1 µÄH2SO4ÓėZn·“Ó¦£¬µ±ZnĶźČ«ČܽāŹ±£¬Éś³ÉµÄĘųĢå£ØæÉŹ¹Ę·ŗģĶŹÉ«£©ŌŚ±ź×¼×“æöĻĀµÄĢå»żĪŖ22.4L£®½«ĖłµĆµÄČÜŅŗĻ”ŹĶ³É1L£¬²āµĆČÜŅŗH+µÄÅضČĪŖ1molL©1£¬ŌņĖłÉś³ÉµÄĘųĢåÖŠSO2ÓėH2µÄĢå»ż±ČŌ¼ĪŖ£Ø £©
A£®1£ŗ2 B£®2£ŗ1 C£®1£ŗ4 D£®4£ŗ1
”¾“š°ø”æA
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗÓÉĢāŅāæÉÖŖ£¬ÅØĮņĖįÓėZn·“Ó¦²śÉśSO2£¬Ėę×Å·“Ó¦µÄ½ųŠŠ£¬H2SO4ÅØ¶Č½µµĶ£¬ŌŚ½ĻĻ”µÄČÜŅŗÖŠ£¬H2SO4ÓėZn·“Ó¦²śÉśH2£ŗZn£«2H2SO4£ØÅØ£©==ZnSO4£«SO2”ü£«2H2O£¬Zn£«H2SO4==ZnSO4£«H2”ü£¬SO2ŗĶH2µÄ»ģŗĻĘųĢåĪŖ1 mol£¬ČōÓŠx mol SO2£¬ŌņÓŠ£Ø1-x£©mol H2£¬Éś³ÉSO2ĻūŗÄH2SO42x mol£¬Éś³ÉH2ĻūŗÄH2SO4£Ø1-x£©mol”£![]() £¬x=0.33,1-x=0.67”£ n£ØSO2£©”Ćn£ØH2£©£½0.33 mol”Ć0.67 mol£½1”Ć2£¬øł¾Ż°¢·ü¼ÓµĀĀŽ¶ØĀÉÖŖ£¬V£ØSO2£©”ĆV£ØH2£©£½1”Ć2£¬“š°øŃ”A”£
£¬x=0.33,1-x=0.67”£ n£ØSO2£©”Ćn£ØH2£©£½0.33 mol”Ć0.67 mol£½1”Ć2£¬øł¾Ż°¢·ü¼ÓµĀĀŽ¶ØĀÉÖŖ£¬V£ØSO2£©”ĆV£ØH2£©£½1”Ć2£¬“š°øŃ”A”£


 æŚĖ抔דŌŖæŚĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø
æŚĖ抔דŌŖæŚĖćĖŁĖćĢģĢģĮ·ĻµĮŠ“š°ø ĢģĢģĮ·æŚĖćĻµĮŠ“š°ø
ĢģĢģĮ·æŚĖćĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĶ¬Ń§½ųŠŠ¼ŅĶ„Š”ŹµŃ飬½«Ń”ĻīÖŠµÄĪļÖŹÓėĖ®³ä·Ö»ģŗĻ£¬ĖłµĆ·ÖÉ¢Ļµ²»ŹĒČÜŅŗµÄŹĒ£Ø £©
A£®Ź³ŃĪ B£®Ö²ĪļÓĶ C£®ÕįĢĒ D£®¾Ę¾«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫°±Ė®»ŗ»ŗµŲµĪČėŃĪĖįÖŠÖĮÖŠŠŌ£¬ĻĀĮŠÓŠ¹ŲµÄĖµ·Ø£ŗ¢ŁŃĪĖį¹żĮæ ¢Ś°±Ė®¹żĮæ ¢ŪĒ”ŗĆĶźČ«·“Ó¦ ¢Üc(NH4£«)£½c(Cl£) ¢Żc(NH4£«)<c(Cl£)ÕżČ·µÄŹĒ( )
A.¢Ł¢Ż
B.¢Ū¢Ü
C.¢Ś¢Ż
D.¢Ś¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĀČ»ÆĶæÉÓĆÓŚÉś²śŃÕĮĻ”¢Ä¾²Ä·ĄøƼĮµČ£®ÓĆ“ÖĶ£Øŗ¬ŌÓÖŹFe£©¾¹żŅ»ĻµĮŠ²½ÖčæÉÖʱøĀČ»ÆĶ¾§Ģå£ØCuCl22H2O£©£®Ķź³ÉĻĀĮŠĢīæÕ£ŗ
£Ø1£©ŹµŃéŹŅÓĆÅØŃĪĖįŗĶ¶žŃõ»ÆĆĢ¹²ČČĄ“ÖʱøCl2£¬Š“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½______________£®
£Ø2£©¼ÓČėŹŌ¼Į½«CuCl2ŗĶFeCl3µÄ»ģŗĻČÜŅŗpHµ÷ÖĮ4”«5£¬¹żĀĖµĆµ½“æ¾»µÄCuCl2ČÜŅŗ£¬Ó¦¼ÓČėµÄŹŌ¼ĮŹĒ______________£ØĢī×ÖÄø±ąŗÅ£©
a£®CuO b£®NaOH c£®Cu2£ØOH£©2CO3 d£®Cu
£Ø3£©CuCl2ČÜŅŗĶعżÕō·¢”¢½į¾§æɵƵ½CuCl22H2O£®
¢ŁÕō·¢¹ż³ĢÖŠ£¬¼ÓČėŃĪĖįµÄÄæµÄŹĒ______________£®
¢ŚÕō·¢¹ż³ĢÖŠ£¬¹Ū²ģµ½ČÜŅŗŃÕÉ«ÓÉĄ¶É«±äĪŖĀĢÉ«£®
ĘäŌĄķŹĒ£ŗ![]()
ÉĻŹö·“Ó¦µÄ»ÆŃ§Ę½ŗā³£Źż±ķ“ļŹ½ŹĒ______________£®
ÓūŹ¹ČÜŅŗÓÉĀĢÉ«±ä³ÉĄ¶É«µÄ“ėŹ©ŹĒ£ŗa__________£»b__________£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŖĮĖŃŠ¾æĢ¼ĖįøĘÓėŃĪĖį·“Ó¦µÄ·“Ó¦ĖŁĀŹ£¬Ä³Ķ¬Ń§ĶعżČēĶ¼ŹµŃé×°ÖĆ²ā¶Ø·“Ó¦ÖŠÉś³ÉµÄCO2ĘųĢåĢå»ż£¬²¢»ęÖĘ³öČēĶ¼ĖłŹ¾µÄĒśĻß”£Ēė·ÖĪöĢÖĀŪŅŌĻĀĪŹĢā”£
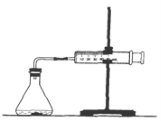
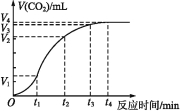
(1)»Æѧ·“Ó¦ĖŁĀŹ×īæģµÄŹ±¼ä¶ĪŹĒ””””””£¬Ó°Ļģ“ĖŹ±¼ä¶Ī·“Ó¦ĖŁĀŹµÄÖ÷ŅŖŅņĖŲŹĒ””””””””””””””””””””””””””””””””””””””””””£»
A£®O~t1 B£®t1~t2 C£®t2~t3 D£®t3~t4
(2)ĪŖĮĖ¼õ»ŗÉĻŹö·“Ó¦ĖŁĀŹ£¬ÓūĻņŃĪĖįÖŠ¼ÓČėĻĀĮŠĪļÖŹ£¬ÄćČĻĪŖæÉŠŠµÄÓŠ””””””£»
A£®ÕōĮóĖ® B£®NaCl¹ĢĢå C£®NaClČÜŅŗ D£®ĶØČėHCl
(3)ČōŃĪĖįµÄĢå»żŹĒ20 mL£¬Ķ¼ÖŠCO2µÄĢå»żŹĒ±ź×¼×“æöĻĀµÄĢå»ż£¬Ōņt1~t2Ź±¼ä¶ĪĘ½¾ł·“Ó¦ĖŁĀŹv(HCl)=””””””mol”¤(L”¤min)-1”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³żČ„Ć¾·ŪÖŠµÄÉŁĮæĀĮ·Ū£¬æÉŃ”ÓĆ£Ø””””£©
A.ĮņĖį
B.°±Ė®
C.ŃĪĖį
D.ĒāŃõ»ÆÄĘČÜŅŗ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒCO2Éś²ś¼×“¼µÄÄÜĮæ±ä»ÆŹ¾ŅāĶ¼£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
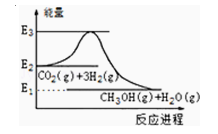
A£®E2_E1ŹĒøĆ·“Ó¦µÄČČŠ§Ó¦
B£®E3_E1ŹĒøĆ·“Ó¦µÄČČŠ§Ó¦
C£®øĆ·“Ó¦·ÅČČ£¬ŌŚ³£ĪĀ³£Ń¹ĻĀ¾ĶÄܽųŠŠ
D£®ŹµĻÖ±ä·ĻĪŖ±¦£¬ĒŅÓŠŠ§æŲÖĘĪĀŹŅŠ§Ó¦
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪ“Ą“ŠĀÄÜŌ“µÄĢŲµćŹĒ׏Ō“·įø»£¬ŌŚŹ¹ÓĆŹ±¶Ō»·¾³ĪŽĪŪČ¾»ņĪŪČ¾ŗÜŠ”£¬ĒŅæÉŅŌŌŁÉś£®ĻĀĮŠŹōÓŚĪ“Ą“ŠĀÄÜŌ“±ź×¼µÄŹĒ£Ø””””£©
¢ŁĢģČ»Ęų ¢ŚĆŗ ¢ŪŗĖÄÜ ¢ÜŹÆÓĶ ¢ŻĢ«ŃōÄÜ ¢ŽÉśĪļÖŹÄÜ ¢ß·ēÄÜ ¢ąĒāÄÜ£®
A.¢Ł¢Ś¢Ū¢Ü
B.¢Ż¢Ž¢ß¢ą
C.¢Ł¢Ū¢Ż¢Ž¢ß¢ą
D.¢Ū¢Ü¢Ż¢Ž¢ß¢ą
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A. ČÜŅŗŗĶ½ŗĢåµÄ±¾ÖŹĒų±šĪŖŹĒ·ńÄܲśÉś¶”“ļ¶ūŠ§Ó¦
B. K2Cr2O7ČÜŅŗŗĶĒāäåĖįÄÜ“ę·ÅÓŚĶ¬Ņ»Ņ©Ę·³÷ÄŚ
C. ÓĆ“ų²£Į§ČūµÄĻøæŚŹŌ¼ĮĘæ±£“ęĒā·śĖį
D. CH4ŗĶC2H4¾łŹōÓŚ³£ÓĆĪ£ĻÕĘ·ÖŠµÄŅ×Č¼ĘųĢå
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com