
| A. | 试剂a可选用酸化的双氧水 | |
| B. | 试剂b可选用酒精 | |
| C. | 步骤③的操作是过滤 | |
| D. | 步骤①需用坩埚,步骤⑤需用分液漏斗 |
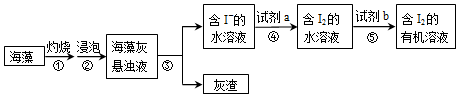
分析 从海藻里提取碘,海藻灼烧后得到海藻灰浸泡后得到海藻灰的浊液,将悬浊液分离为残渣和含碘离子溶液应选择过滤的方法;过滤得到含碘离子的溶液加入氧化剂(如氯气、双氧水等)可氧化碘离子为碘单质,得到含碘水溶液;向含碘单质的水溶液中加入有机溶剂(苯或四氯化碳),萃取分液得到含碘的有机层,通过蒸馏得到碘单质,据此进行解答.
解答 解:A.试剂a的作用是将碘离子氧化成碘单质,可以为双氧水,故A正确;
B.碘单质易溶于酒精,不能用酒精作萃取剂,可以用四氯化碳或苯,故B错误;
C.步骤③的目的是分离海藻灰与溶液,需要通过过滤操作完成,故C正确;
D.步骤①灼烧海藻,需要在坩埚中进行;步骤⑤将有机层与水溶液分离,需要通过分液操作完成,故D正确;
故选B.
点评 本题考查了海水资源的综合应用,题目难度中等,根据实验流程明确实验操作方法为解答关键,注意掌握海水资源及其综合应用方法,试题培养了学生的化学实验能力.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
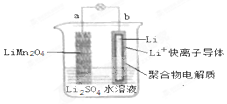 2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系,放电时,该电池的反应为 Li1-xMn2O4+xLi=LiMn2O4.则下列叙述错误的是( )
2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系,放电时,该电池的反应为 Li1-xMn2O4+xLi=LiMn2O4.则下列叙述错误的是( )| A. | a 为电池的正极 | |
| B. | 电池充电反应为 LiMn2O4=Li1-xMn2O4+xLi | |
| C. | 放电时,a 极锂的化合价发生变化 | |
| D. | 放电时,溶液中 Li+从 b 向 a 迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
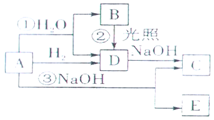 A是黄绿色气体单质,如图所示,
A是黄绿色气体单质,如图所示,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2具有氧化性,能使品红溶液褪色 | |
| B. | SO2具有漂白性,能使溴水褪色 | |
| C. | SO2具有还原性,能与Ba(NO3)2溶液反应生成沉淀 | |
| D. | SO2具有漂白性,能使滴加酚酞的NaOH溶液由红色变为无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 操作 | 现象 |
| 向反应瓶中加入6.5g锌粉,然后加入50mL 1.0mol•L-1的FeCl3溶液,搅拌 | 溶液温度迅速上升,稍后出现红褐色沉淀,同时出现少量气泡;反应一段时间后静置,上层溶液为浅绿色,反应瓶底部有黑色固体 |
| 收集检验反应过程中产生的气体 | 集气管口靠近火焰,有爆鸣声 |
| 操作 | 现象 |
| 将5mL 1.0mol•L-1的FeCl3溶液与0.65g锌粉混合 | 溶液温度迅速上升,开始时几乎没有气泡 |
| 将5 mL 0.2 mol•L-1(或pH=0.7)的盐酸与0.65g锌粉混合 | 溶液中立即产生大量气泡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑥⑦ | B. | ①②⑤⑦ | C. | ②④⑥ | D. | ②④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 分类标准 | 分类结果 |
| A | 根据化学反应中有无单质参加或生成 | 氧化还原反应和非氧化还原反应 |
| B | 根据化学反应中有无离子参加或生成 | 离子反应和非离子反应 |
| C | 根据混合物中分散质粒子直径的大小 | 胶体、溶液和浊液 |
| D | 根据无机化合物的组成和性质特点 | 酸、碱、盐、氧化物等 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com