
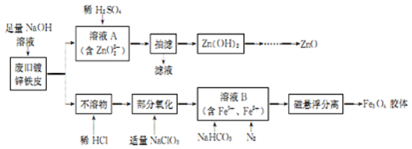
���� �Ͼɶ�п��Ƥ��������������Һ�з�Ӧ��п�ܽ�����ƫп���ƺ������������ܽ⣬���˵õ���ҺAΪNa2ZnO2��������ΪFe����ҺA��ϡ����ʹ��Һ��ZnO22-ת��ΪZn��OH��2�������پ������ˡ�ϴ�ӡ�������յõ�ZnO��
������Fe�м���ϡ���ᣬ��Ӧ�����Ȼ���������������NaClO3������������������Ϊ�����ӣ��õ���Fe2+��Fe3+��B��Һ���ټ���NaHCO3����ͨ�뵪�������������������������ӣ��ݴ˷������
��� �⣺��1����ҺA��пת��Ϊп���ƣ�Na2ZnO2������п������������Һ��Ӧ����ƫп���ƺ���������Ӧ�Ļ�ѧ����ʽΪ��Zn+2NaOH=Na2ZnO2+H2����
�ʴ�Ϊ��Zn+2NaOH=Na2ZnO2+H2����
��2������ҺA�еμ�ϡH2SO4���������ܽ������Zn��OH��2��ѡ�����ᣬ��ͨ�����CO2��
�ʴ�Ϊ��ͨ�����CO2��
����Zn��OH��2������ZnOǰ�����ϴ�ӣ�����渽����������ӣ�������������Ӽ��ɣ�����Ϊ��ȡ�������һ�ε�ϴ����Һ���Թ��У������еμ������ữ��BaCl2��Һ������������ɫ�����������������ϴ�Ӹɾ���
�ʴ�Ϊ��ȡ�������һ�ε�ϴ����Һ���Թ��У������еμ������ữ��BaCl2��Һ������������ɫ�����������������ϴ�Ӹɾ���
��3�������м���NaClO3����������������Ϊ�����ӣ�������ӦΪ6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O��
�ʴ�Ϊ��6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O��
��4���ٷ�ֹFe2+������������ҺB�Ƶ�Fe3O4�������ӵĹ�����ͨ��N2��
�ʴ�Ϊ����ֹFe2+��������
����ҺBΪ��Fe2+��Fe3+����Һ������NaHCO3�����������������������ӣ����ӷ���ʽΪ��Fe2++Fe3++8HCO3-=Fe3O4�����壩+8CO2��+4H2O��
�ʴ�Ϊ��Fe2++Fe3++8HCO3-=Fe3O4�����壩+8CO2��+4H2O��
�ۼ����������ӿ����仹ԭ�ԣ�����Ϊ��ȡ����B��Һ���μ�KMnO4��Һ�����ϣ���ɫ��ȥ��
�ʴ�Ϊ��ȡ����B��Һ���μ�KMnO4��Һ�����ϣ���ɫ��ȥ��
���� ���������ʵ��Ʊ�Ϊ���壬����ʵ����������ͼ��ܣ�����Ϣ�����á�ʵ�������Ŀ��Ƶȣ������Ѷ��еȣ��Ƕ�ѧ���ۺ������Ŀ��飬��Ҫѧ������֪ʶ�Ļ�����������⡢��������������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1 mol | B�� | 0.5 mot | C�� | 0.25 mol | D�� | 0.125 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 8�� | B�� | 9�� | C�� | 10�� | D�� | 11�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 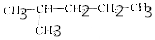 �� ��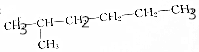 | |
| B�� | 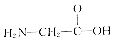 ��CH3-CH2-NO2 ��CH3-CH2-NO2 | |
| C�� | CH3-CH2-CH2-COOH��CH3-CH2-CH2-CH2-COOH | |
| D�� | CH3-CH2-O-CH2-CH3��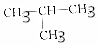 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
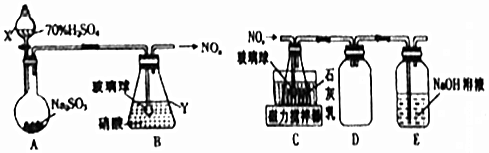
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
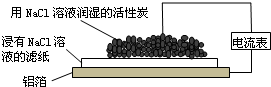
| A�� | ����Ϊ����������������Ӧ������ʴ | |
| B�� | ������ӦΪ2H2O+O2+4e-�T4OH- | |
| C�� | Cl-�ɻ���̿��������������Ǩ�ƣ������������������� | |
| D�� | �װߵ���Ҫ�ɷֿ�����Al2O3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | ��ʼ����pH | ������ȫpH |
| Fe2+ | 7.6 | 9.6 |
| Fe3+ | 2.7 | 3.7 |
| Zn2+ | 5.4 | 8.0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ܽ�ȣ�С�մ��մ� | B�� | �е㣺K��Na | ||
| C�� | �ܶȣ��壾ˮ | D�� | ���ȶ��ԣ�HF��HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2��HCl����ͨ��ˮϴ�� | B�� | NO��NH3����ͨ��ˮϴ�� | ||
| C�� | NH4Cl��I2�������Ȼ���� | D�� | NH4Cl��Һ��I2������CCl4��ȡ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com