
| A. | 乙炔的结构简式CHCH | B. | 羟基的电子式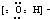 | ||
| C. | 乙酸的分子式C2H4O2 | D. | 乙醇的结构式CH3CH2OH |
分析 A.烃的结构简式中不饱和键碳碳双键、碳碳三键不能省略;
B.羟基为中性原子团,电子式中不能标出电荷;
C.乙酸由甲基连接羧基构成;
D.CH3CH2OH为结构简式,结构式需要用短线代替所有的共用电子对.
解答 解:A.乙炔结构简式中碳碳三键不能省略,其结构简式为CH≡CH,故A错误;
B.羟基中氧原子最外层为7个电子,氢原子最外层2个电子,羟基正确的电子式为: ,故B错误;
,故B错误;
C.乙酸由甲基连接羧基构成,结构简式为CH3COOH,分子式为C2H4O2,故C正确;
D.乙醇的结构简式为C2H5OH,则乙醇正确的结构式为: ,故D错误;
,故D错误;
故选C.
点评 本题考查了常见化学用语的书写方法,题目难度中等,注意掌握结构式、结构简式、电子式、分子式等化学用语的概念及书写原则,试题培养了学生规范答题的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 降低温度 | B. | 增大压强 | C. | 充入一定量CO2 | D. | 再加入一些铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2 CH2CH3 | B. | CH3COOCH2CH3 | C. | CH3CH2COOH | D. | CH3CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制备乙酸乙酯的实验中,承接酯的小试管中盛放了一定量的氢氧化钠溶液 | |
| B. | 实验室制乙烯时应将无水乙醇缓慢加入到浓硫酸中 | |
| C. | 在酸性重铬酸钾溶液中加入少量乙醇,橙色溶液变红 | |
| D. | 为减缓反应速率,将饱和食盐水滴加到烧瓶中的电石上来制取乙炔 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.3mol氢气中含有氢原子的数目为0.3NA | |
| B. | 标准状况下,4.48L苯中含有苯分子的数目为0.2NA | |
| C. | 0.2mol•L-1CaCl2溶液中含有氯离子的数目为0.4NA | |
| D. | 1molNa2O2与足量水反应,转移的电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com