
| ���� | ���볣�� |
| CH3COOH | K=1.75��10-5 |
| H2CO3 | K1=4.4��10-7 k2=4.7��10-11 |
| HClO | K=3.2��10-8 |
| A�� | �ڣ��ܣ��ۣ��� | B�� | �٣��ۣ��ܣ��� | C�� | �ۣ��ڣ��ܣ��� | D�� | �ۣ��ܣ��ڣ��� |
���� ��ˮ��������Ӷ�Ӧ�������Խ�������ε�ˮ��̶�Խ����Һ�ļ���Խǿ����ҺpHԽ��
��� �⣺�����ʵ���Ũ�Ȣ�CH3COONa��Һ��Na2CO3��Һ��NaHCO3��Һ��NaClO��Һ����֪���ԣ�CH3COOH��H2CO3��HClO��HCO3-������ˮ��̶ȣ�CH3COONa��NaHCO3��NaClO��Na2CO3����Һ��pH�ɴ�С��˳��NaClO��NaHCO3��CH3COONa�����ڣ��ܣ��ۣ��٣�
��ѡA��
���� ���⿼��ѧ���ε�ˮ��ԭ����Ӧ��֪ʶ��ע��֪ʶ��Ǩ��Ӧ���ǹؼ����Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
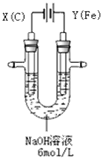 ������أ�K2FeO4�����и�Ч���������ã�Ϊһ�����ͷ��ȸ�Ч����������ⷨ�Ʊ�������ز�����㣬�ɹ��ʸߣ�����ʵ�����Ʊ�����ԭ����ͼ��ʾ��
������أ�K2FeO4�����и�Ч���������ã�Ϊһ�����ͷ��ȸ�Ч����������ⷨ�Ʊ�������ز�����㣬�ɹ��ʸߣ�����ʵ�����Ʊ�����ԭ����ͼ��ʾ�� �鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢޢ� | B�� | �٢ڢۢ� | C�� | �ڢޢ�� | D�� | �ۢݢޢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CO2��NaOH��Һ | B�� | SO2��ϡ��ˮ | C�� | NO2��NaOH��Һ | D�� | Cl2�ͱ���ʳ��ˮ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
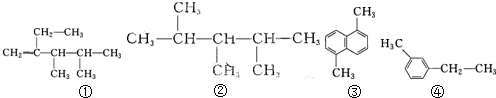
| A�� | �٢� | B�� | �ۢ� | C�� | �ڢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1mol | B�� | 1.6mol | C�� | 2.2mol | D�� | 2.4mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
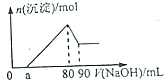 Fe2O3��Al2O3�Ļ������ȫ�ܽ���160mL2mol/LHCl��Һ�У���������Һ�еμ�NaOH��Һ�õ���ͼ������˵������ȷ���ǣ�������
Fe2O3��Al2O3�Ļ������ȫ�ܽ���160mL2mol/LHCl��Һ�У���������Һ�еμ�NaOH��Һ�õ���ͼ������˵������ȷ���ǣ�������| A�� | ��a=20mLʱ����������Fe2O3ռ0.02mol | |
| B�� | ���μӵ�Na0H��Һ��Ũ��Ϊ4mol/L | |
| C�� | a�㴦��Na0H��Һ�����Ϊa��50mL | |
| D�� | ��a=20mL����ʣ����������Ϊ20mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaOH��Һ | B�� | AgNO3��Һ | C�� | Ba��OH��2��Һ | D�� | BaCl2��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com