
Ζ÷Έω Θ®1Θ©CeO2‘ΎœΓΝρΥαΚΆH2O2ΒΡΉς”Οœ¬Ω……ζ≥…Ce3+Θ§CeO2÷–ΒΡCe «+4ΦέΘ§‘ΎH2O2ΒΡΉς”Οœ¬Ω……ζ≥…Ce3+Θ§“ρ¥ΥΖΔ…ζΜΙ‘≠Ζ¥”ΠΘ§CeO2‘ΎΗΟΖ¥”Π÷–Ής―θΜ·ΦΝΘΜ
Θ®2Θ©Ή‘»ΜΫγ÷–Cr÷ς“Σ“‘+3ΦέΚΆ+6Φέ¥φ‘ΎΘ°+6ΦέΒΡCrΡή“ΐΤπœΗΑϊΒΡΆΜ±δΘ§Ω…“‘”Ο―«ΝρΥαΡΤΫΪΤδΜΙ‘≠ΈΣ+3ΦέΒΡΗθΘ§ΗυΨίΒΟ ßΒγΉ”œύΒ»Θ§Cr2O72-”κSO32-ΒΡΈο÷ ΒΡΝΩ÷°±» «1ΘΚ3ΘΜΫαΚœ‘≠Ή” ΊΚψΚΆΒγΚ… ΊΚψ≈δΤΫ ι–¥άκΉ”ΖΫ≥Χ ΫΘΜ
Θ®3Θ©ΙΛ“Β…œ‘Ύ550Γφ ±”ΟΡΤ”κΥΡ¬»Μ·ν―Ζ¥”ΠΩ…÷ΤΒΟν―Θ§ΥΡ¬»Μ·ν―±ΜΡΤΜΙ‘≠ΈΣν―Θ§“άΨί‘≠Ή” ΊΚψ ι–¥ΘΜ
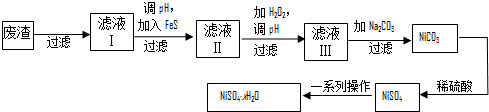
Θ®4Θ©ΒγΕΤΖœ‘ϋΘ®≥ΐΡχΆβΘ§ΜΙΚ§”–Ά≠ΓΔ–ΩΓΔΧζΒ»‘ΣΥΊΘ©Θ§Ιΐ¬ΥΚσ‘Ύ¬Υ“Κ÷–Φ”»κFeSΘ§…ζ≥…CuSΓΔZnSΘ§Ω…≥ΐ»ΞCu2+ΓΔZn2+Β»‘”÷ Θ§Ε‘¬Υ“ΚΔρœ»Φ”WΘ§”ΠΈΣΙΐ―θΜ·«βΘ§Ω…―θΜ·Fe2+…ζ≥…Fe3+Θ§”–άϊ”ΎΥ°Ϋβ…ζ≥…«β―θΜ·Χζ≥ΝΒμΕχ≥ΐ»ΞΘ§Ιΐ¬ΥΚσ‘Ύ¬Υ“Κ÷–Φ”»κΧΦΥαΡΤΘ§Ω……ζ≥…NiCO3Θ§Ιΐ¬ΥΚσΦ”»κΝρΥαΩ……ζ≥…NiSO4Θ§Ψ≠’τΖΔΓΔ≈®ΥθΓΔά以ΫαΨßΩ…ΒΟΒΫΝρΥαΡχΨßΧεΘ§“‘¥ΥΫβ¥πΘ°
Ϋβ¥π ΫβΘΚΘ®1Θ©CeO2‘ΎœΓΝρΥαΚΆH2O2ΒΡΉς”Οœ¬Ω……ζ≥…Ce3+Θ§CeO2÷–ΒΡCe «+4ΦέΘ§‘ΎH2O2ΒΡΉς”Οœ¬Ω……ζ≥…Ce3+Θ§“ρ¥ΥΖΔ…ζΜΙ‘≠Ζ¥”ΠΘ§CeO2‘ΎΗΟΖ¥”Π÷–Ής―θΜ·ΦΝΘ§Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ2CeO2+H2O2+6H+=2Cr3++O2Γϋ+4H2OΘ§
Ι ¥πΑΗΈΣΘΚ2CeO2+H2O2+6H+=2Cr3++O2Γϋ+4H2OΘΜ―θΜ·ΘΜ
Θ®2Θ©Ή‘»ΜΫγ÷–Cr÷ς“Σ“‘+3ΦέΚΆ+6Φέ¥φ‘ΎΘ°+6ΦέΒΡCrΡή“ΐΤπœΗΑϊΒΡΆΜ±δΘ§Ω…“‘”Ο―«ΝρΥαΡΤΫΪΤδΜΙ‘≠ΈΣ+3ΦέΒΡΗθΘ§ΗυΨίΒΟ ßΒγΉ”œύΒ»Θ§Cr2O72-”κSO32-ΒΡΈο÷ ΒΡΝΩ÷°±» «1ΘΚ3ΘΜΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΘΚCr2O72-+3SO32-+8H+=2Cr3++3SO42-+4H2OΘ§
Ι ¥πΑΗΈΣΘΚCr2O72-+3SO32-+8H+=2Cr3++3SO42-+4H2OΘΜ
Θ®3Θ©ΙΛ“Β…œ‘Ύ550Γφ ±”ΟΡΤ”κΥΡ¬»Μ·ν―Ζ¥”ΠΩ…÷ΤΒΟν―Θ§ΥΡ¬»Μ·ν―±ΜΡΤΜΙ‘≠ΈΣν―Θ§Ζ¥”ΠΒΡΜ·―ßΖΫ≥Χ ΫΈΣΘΚ4Na+TiCl4®TTi+4NaClΘ§
Ι ¥πΑΗΈΣΘΚ4Na+TiCl4®TTi+4NaClΘΜ
Θ®4Θ©ΒγΕΤΖœ‘ϋΘ®≥ΐΡχΆβΘ§ΜΙΚ§”–Ά≠ΓΔ–ΩΓΔΧζΒ»‘ΣΥΊΘ©Θ§Ιΐ¬ΥΚσ‘Ύ¬Υ“Κ÷–Φ”»κFeSΘ§…ζ≥…CuSΓΔZnSΘ§Ω…≥ΐ»ΞCu2+ΓΔZn2+Β»‘”÷ Θ§Ε‘¬Υ“ΚΔρœ»Φ”WΘ§”ΠΈΣΙΐ―θΜ·«βΘ§Ω…―θΜ·Fe2+…ζ≥…Fe3+Θ§”–άϊ”ΎΥ°Ϋβ…ζ≥…«β―θΜ·Χζ≥ΝΒμΕχ≥ΐ»ΞΘ§Ιΐ¬ΥΚσ‘Ύ¬Υ“Κ÷–Φ”»κΧΦΥαΡΤΘ§Ω……ζ≥…NiCO3Θ§Ιΐ¬ΥΚσΦ”»κΝρΥαΩ……ζ≥…NiSO4Θ§Ψ≠’τΖΔΓΔ≈®ΥθΓΔά以ΫαΨßΩ…ΒΟΒΫΝρΥαΡχΨßΧεΘ§
ΔΌFeS≥ΐ»ΞCu2+ΒΡΖ¥”Π «≥ΝΒμΒΡΉΣΜ·Θ§Φ¥FeS+Cu2+=CuS+Fe2+Θ§
Ι ¥πΑΗΈΣΘΚFeS+Cu2+=CuS+Fe2+ΘΜ
ΔΎΕ‘¬Υ“ΚΔρΦ”H2O2ΒΡΡΩΒΡ «ΫΪFe2+―θΜ·Fe3+Θ§»ΜΚσΒςpH≥ΝΒμFe3+Θ§
Ι ¥πΑΗΈΣΘΚ―θΜ·Fe2+ΘΜ≥ΐ»ΞFe3+ΘΜ
ΔέNiSO4”κNa2CO3Ζ¥”Π…ζ≥…NiCO3≥ΝΒμΘ§ΕχΚσΙΐ¬ΥΘ§‘ΌΦ” ΝΩœΓΝρΥα»ήΫβ”÷…ζ≥…NiSO4Θ§’β―υΩ…ΧαΗΏNiSO4ΒΡ≈®Ε»Θ§”–άϊ”Ύ’τΖΔΫαΨßΘ§
Ι ¥πΑΗΈΣΘΚ‘ω¥σNiSO4ΒΡ≈®Ε»Θ§άϊ”Ύ’τΖΔΫαΨßΘ®ΜρΗΜΦ·NiSO4Θ©Θ°
ΒψΤά ±ΨΧβΩΦ≤ιΫœΈΣΉέΚœΘ§…φΦΑ―θΜ·ΜΙ‘≠Ζ¥”ΠΓΔ―ΈάύΒΡΥ°ΫβΓΔΈο÷ ΒΡΖ÷άκΧα¥Ω“‘ΦΑ‘≠Βγ≥Ί÷Σ ΕΘ§ΈΣΗΏΤΒΩΦΒψΘ§≤ύ÷Ί”Ύ―ß…ζΒΡΖ÷ΈωΡήΝΠΚΆ Β―ιΡήΝΠΒΡΩΦ≤ιΘ§ΈΣΗΏΤΒΩΦΒψΚΆ≥ΘΦϊΧβ–ΆΘ§ΧβΡΩΡ―Ε»÷–Β»Θ§ΉΔ“βΑ―Έ’Μυ¥Γ÷Σ ΕΒΡΜΐάέΘ°



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
| AΘ° | …’±≠÷–“ΜΕ®”–Ά≠Θ§Ω…Ρή”–Χζ | |
| BΘ° | …’±≠÷–ΧζΆ≠ΕΦ”– | |
| CΘ° | »ή“Κ÷–“ΜΕ®”–Fe2+Θ§Ω…Ρή”–Cu2+ΓΔFe3+ | |
| DΘ° | …’±≠÷–”–ΧζΈόΆ≠ |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΧνΩ’Χβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΫβ¥πΧβ
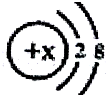 Β±x=8 ±Θ§ΗΟΝΘΉ”ΖϊΚ≈ΈΣO2-ΘΜΒ±x=11 ±Θ§ΗΟΝΘΉ”ΖϊΚ≈ΈΣNa+ΘΜΒ±x=13 ±Θ§–¥≥ωΗΟΝΘΉ”ΒΡœθΥα―ΈΒΡΜ·―ß ΫΈΣΘΚAlΘ®NO3Θ©3Θ°
Β±x=8 ±Θ§ΗΟΝΘΉ”ΖϊΚ≈ΈΣO2-ΘΜΒ±x=11 ±Θ§ΗΟΝΘΉ”ΖϊΚ≈ΈΣNa+ΘΜΒ±x=13 ±Θ§–¥≥ωΗΟΝΘΉ”ΒΡœθΥα―ΈΒΡΜ·―ß ΫΈΣΘΚAlΘ®NO3Θ©3Θ°≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΫβ¥πΧβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
| AΘ° | KOH | BΘ° | LiCl | CΘ° | H2 | DΘ° | NH3 |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ―Γ‘ώΧβ
| AΘ° | Υ°’τΤχ | BΘ° | ¬»Μ·ΡΤ | CΘ° | ΝρΥα | DΘ° | «β―θΜ·ΡΤ |
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΧνΩ’Χβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚΦΤΥψΧβ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com