
| A£® | ·“Ó¦¢ŪÖŠBr2 ŹĒŃõ»Æ¼Į£¬äåŌŖĖŲ±»Ńõ»Æ | |
| B£® | Ńõ»ÆŠŌĒæČõĖ³ŠņĪŖ£ŗMnO4-£¾Cl2£¾Fe3+£¾Br2 | |
| C£® | ·“Ó¦¢ŁÖŠ£¬±»Ńõ»ÆµÄHClÕ¼²Ī¼Ó·“Ó¦µÄHClµÄ5/8 | |
| D£® | ČÜŅŗÖŠæÉ·¢Éś·“Ó¦£ŗ2Fe3++2Cl-=2Fe2++Cl2”ü |
·ÖĪö A”¢Ėłŗ¬ŌŖĖŲ»ÆŗĻ¼Ū½µµĶµÄĪļÖŹĪŖŃõ»Æ¼Į£¬»ÆŗĻ¼ŪÉżøßµÄŌŖĖŲ±»Ńõ»Æ£»
B”¢Ķ¬Ņ»»Æѧ·“Ó¦ÖŠŃõ»Æ¼ĮµÄŃõ»ÆŠŌ“óÓŚŃõ»Æ²śĪļµÄŃõ»ÆŠŌ£»
C”¢HClÖŠ²æ·ÖClŌŖĖŲ±ä¼Ū£¬øł¾ŻÉś³ÉµÄCl2ŹżÄæÅŠ¶Ļ£»
D”¢øł¾ŻŃõ»ÆŠŌĒæČõÅŠ¶Ļ·“Ó¦ÄÜ·ń·¢Éś£®
½ā“š ½ā£ŗA”¢Ėłŗ¬ŌŖĖŲ»ÆŗĻ¼Ū½µµĶµÄĪļÖŹĪŖŃõ»Æ¼Į£¬»ÆŗĻ¼ŪÉżøßµÄŌŖĖŲ±»Ńõ»Æ£¬Ōņ·“Ó¦¢ŪÖŠBr2 ŹĒŃõ»Æ¼Į£¬äåŌŖĖŲµÄ»ÆŗĻ¼Ū½µµĶ±»»¹Ō£¬¹ŹA“ķĪó£»
B”¢¢Ł2KMnO4+16HClØT2KCl+2MnCl2+5Cl2”ü+8H2OÖŠKMnO4µÄŃõ»ÆŠŌ“óÓŚCl2£¬¢ŚCl2+2NaBrØT2NaCl+Br2 ÖŠCl2µÄŃõ»ÆŠŌ“óÓŚBr2£¬¢Ū2Fe2++Br2=2 Fe3++2Br- ÖŠBr2µÄŃõ»ÆŠŌ“óÓŚFe3+£¬ĖłŅŌŃõ»ÆŠŌ“óŠ”Ė³ŠņĪŖ£ŗMnO4-£¾Cl2£¾Br2£¾Fe3+£¬¹ŹB“ķĪó£»
C”¢2KMnO4+16HClØT2KCl+2MnCl2+5Cl2”ü+8H2O·“Ó¦ÖŠ16øöHClÖŠµÄ10øöHCl±»Ńõ»ÆÉś³É5øöCl2£¬»¹ÓŠ6øöHClĆ»±»Ńõ»Æ£¬ĖłŅŌ±»Ńõ»ÆµÄHClÕ¼²Ī¼Ó·“Ó¦µÄHClµÄ$\frac{5}{8}$£¬¹ŹCÕżČ·£»
D”¢ÓÉBĻī·ÖĪöæÉÖŖ£¬Ńõ»ÆŠŌ£ŗCl2£¾Fe3+£¬ŌņFe3+²»ÄÜŃõ»ÆHCl£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĮĖŃõ»ÆŠŌ”¢»¹ŌŠŌĒæČõµÄÅŠ¶Ļ£¬øł¾Ż”°Ķ¬Ņ»»Æѧ·“Ó¦ÖŠŃõ»Æ¼ĮµÄŃõ»ÆŠŌ“óÓŚŃõ»Æ²śĪļµÄŃõ»ÆŠŌ£¬»¹Ō¼ĮµÄ»¹ŌŠŌ“óÓŚ»¹Ō²śĪļµÄ»¹ŌŠŌ”±¼“æÉ·ÖĪö½ā“š±¾Ģā£¬ÄŃ¶Č²»“ó£®


 Ņ»ĻßĆūŹ¦ĢįÓÅŹŌ¾ķĻµĮŠ“š°ø
Ņ»ĻßĆūŹ¦ĢįÓÅŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĻņĆ÷·Æ£ØKAl£ØSO4£©2•12H2O£©ČÜŅŗÖŠµĪ¼ÓBa£ØOH£©2ČÜŅŗ£¬Ē”ŗĆŹ¹SO42-³ĮµķĶźČ«£ŗ2Al3++3SO42-+3Ba2++6OH-ØT2Al£ØOH£©3”ż+3BaSO4”ż | |
| B£® | Fe3O4ČÜÓŚ×ćĮæĻ”HNO3£ŗFe3O4+8H+=Fe2++2Fe3++4H2O | |
| C£® | ²£Į§ŹŌ¼ĮĘæ±»ÉÕ¼īČÜŅŗøÆŹ“£ŗSiO2+2Na++2OH-=Na2SiO3”ż+H2O | |
| D£® | VO2+ÓėĖįŠŌøßĆĢĖį¼ŲČÜŅŗ·“Ó¦£ŗ5VO2++MnO4-+H2OØT5VO2++Mn2++2H+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ĪļÖŹ | Ėłŗ¬ŌÓÖŹ | ³żČ„ŌÓÖŹµÄ·½·Ø | |
| A | COĘųĢå | CO2 | Ķعż×ćĮæĒāŃõ»ÆÄĘČÜŅŗ£¬²¢øÉŌļ |
| B | NaOHČÜŅŗ | Na2CO3 | ¼ÓČė×ćĮæĻ”ŃĪĖįÖĮ²»ŌŁ²śÉśĘųÅŻ |
| C | CaO¹ĢĢå | CaCO3 | ¼ÓĖ®Čܽā£¬¹żĀĖ |
| D | FeSO4ČÜŅŗ | CuSO4 | ¼ÓČė×ćĮæŠæĮ££¬³ä·Ö·“Ó¦£¬¹żĀĖ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Na+ K+ SO42- HCO3- | B£® | Cu2+ K+ SO42- NO3- | ||
| C£® | Na+ K+Cl- NO3- | D£® | Fe3+ K+ SO42- Cl- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ¼×“¼ŹĒŅ»ÖÖæÉŌŁÉśÄÜŌ“£¬¾ßÓŠæŖ·¢ŗĶÓ¦ÓĆµÄ¹ćĄ«Ē°¾°£¬Ēė»Ų“šĻĀĮŠĪŹĢā
¼×“¼ŹĒŅ»ÖÖæÉŌŁÉśÄÜŌ“£¬¾ßÓŠæŖ·¢ŗĶÓ¦ÓĆµÄ¹ćĄ«Ē°¾°£¬Ēė»Ų“šĻĀĮŠĪŹĢā²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| »Æѧ·“Ó¦ | “߻ƼĮ | Ea/KJ•mol-1 | k£Ø“ߣ©/k£ØĪŽ£© | |
| ĪŽ“߻ƼĮ | ÓŠ“߻ƼĮ | |||
| C12H22O11£ØÕįĢĒ£©+H2OØT C6H12O6 £ØĘĻĢŃĢĒ£©+C6H12O6£Ø¹ūĢĒ£© | ÕįĢĒĆø | 107 | 36 | 9.2”Į1011£Ø310K£© |
| 2HIØTH2+I2 | ½š | 184 | 105 | 1.6”Į108£Ø503K£© |
| CH3CHOØTCH4+CO | µā | 210 | 136 | 7.5”Į104£Ø793K£© |
| 2H2O2ØT2H2O+O2 | ¹żŃõ»ÆĒāĆø | 75 | 25 | 5.8”Į108£Ø298K£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | Źµ Ńé | ĻÖ Ļó |
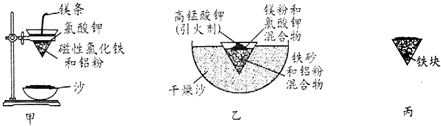
| A | ¼ÓČČ·ÅŌŚŪįŪöÖŠµÄŠ”æéÄĘ | ÄĘĻČČŪ»Æ³É¹āĮĮµÄŠ”Ēņ£¬Č¼ÉÕŹ±£¬»šŃęĪŖ»ĘÉ«£¬Č¼ÉÕŗó£¬Éś³Éµ»ĘÉ«¹ĢĢå |
| B | ŌŚ¾Ę¾«µĘÉĻ¼ÓČČĀĮ² | ĀĮ²ČŪ»Æ£¬Ź§Č„¹āŌó£¬ČŪ»ÆµÄĀĮ²¢²»µĪĀ䣬ŗĆĻńÓŠŅ»²ćĤ¶µ×Å |
| C | ŌŚFeCl2ČÜŅŗÖŠµĪČėNaOHČÜŅŗ | ĻČÉś³É°×É«³Įµķ£¬³ĮµķŗÜæģ±äĪŖ»ŅĀĢÉ«£¬×īŗó±äĪŖŗģŗÖÉ« |
| D | ŌŚæÕĘųÖŠ¾ĆÖƵÄĀĮĢõ·ÅČėNaOHČÜŅŗÖŠ | Į¢æĢ²śÉś“óĮæĪŽÉ«ĘųÅŻ£¬ĀĮĢõÖš½„±äĻø£¬ĀĮĢõÖš½„·¢ČČ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒąŹÆĆŽŹĒŅ»ÖÖ¹čĖįŃĪ²ÄĮĻ | |
| B£® | ĒąŹÆĆŽÖŠŗ¬ÓŠŅ»¶ØĮæµÄŹÆÓ¢¾§Ģå | |
| C£® | ĒąŹÆĆŽµÄ»Æѧ×é³ÉæɱķŹ¾ĪŖNa2O•3FeO•Fe2O3•8SiO2•H2O | |
| D£® | 1molĒąŹÆĆŽÄÜŹ¹1molHNO3±»»¹Ō |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
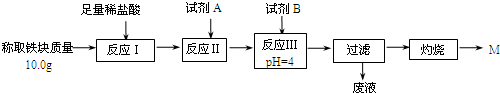
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| æŖŹ¼³ĮµķŹ±µÄpH | 7.5 | 2.8 | 4.2 | 9.6 |
| ³ĮµķĶźČ«Ź±µÄpH | 9.0 | 4.0 | 5 | 11 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com