
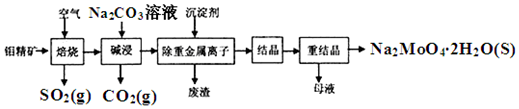
���� �����⾫��MoS2ȼ�գ���Ӧ����ʽΪ2MoS2+7O2$\frac{\underline{\;\;��\;\;}}{\;}$2MoO3+4SO2�����������£�MoO3��Na2CO3��Һ��Ӧ����Ӧ����ʽΪMoO3+CO32-=MoO42-+CO2����Ȼ������Һ�м����������ȥ�ؽ������ӣ���Һ�е�����ΪNa2MoO4������Һ����Ũ������ȴ�ᾧ��Ȼ���ؽᾧ�õ�Na2MoO4.2H2O��
��1�������ڻ��������������ϼ۴�����Ϊ����㣻
��2������ʱΪ��ʹ�⾫���ַ�Ӧ�����⾫���������Ӵ�������������������������Ӧ��Ӵ�ʱ��Խ������ӦԽ��֣�
��3�����չ������⾫��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ��2MoS2+7O2$\frac{\underline{\;\;��\;\;}}{\;}$2MoO3+4SO2��Ԫ�ػ��ϼ����ߵ�ʧȥ���ӷ���������Ӧ�õ�����������ݻ�ѧ����ʽ������ϵ�������ת�����ʵ�����
��4�����������£�MoO3��Na2CO3��Һ��Ӧ���ɶ�����̼�������ƣ�
��� �⣺��1������ᾧˮ��������������Ԫ�صĻ��ϼ�ֻ����Na2MoO4����Ԫ�صĻ��ϼۼ��ɣ���Ԫ����+1����Ԫ����-2������Ԫ�صĻ��ϼ���x�������ڻ��������������ϼ۴�����Ϊ�㣬��֪�����ƣ�Na2MoO4•2H2O������Ԫ�صĻ��ϼۣ���+1����2+x+��-2����4=0����x=+6��
�ʴ�Ϊ��+6��
��2����Ӧ��Ӵ�ʱ��Խ������ӦԽ��֣����յĹ����в��á��������ա��Ĵ�ʩ�������ʯ�����ӿ���ͨ�����ȣ������⾫��������Ӵ���ʹ���ַ�Ӧ�����ԭ�ϵ������ʣ�
�ʴ�Ϊ������ʯ���飨�����ӿ����Ľ��������������ԭ���ȣ���
��3�����չ������⾫��������Ҫ��Ӧ�Ļ�ѧ����ʽΪ��2MoS2+7O2$\frac{\underline{\;\;��\;\;}}{\;}$2MoO3+4SO2��Ԫ�ػ��ϼ����ߵ�ʧȥ���ӷ���������Ӧ�õ����������Ӧ��MoԪ�ػ��ϼ�+2�۱仯Ϊ+6�ۣ���Ԫ�ػ��ϼ�-1�۱仯Ϊ+4�ۣ��÷�Ӧ������������MoO3��SO2����Ӧ������4mol�����������ת��28mol��������1mol�����������ת��Ϊ7mol��
�ʴ�Ϊ��MoO3��SO2��7��
��4�����������£�MoO3��Na2CO3��Һ��Ӧ���ɶ�����̼�������ƣ����ӷ���ʽΪMoO3+CO32-=MoO42-+CO2����
�ʴ�Ϊ��MoO3+CO32-=MoO42-+CO2����
���� ���⿼�����ʵ��Ʊ��Լ����ʷ�����ᴿ�ķ����ͻ��������ۺ�Ӧ�ã�Ϊ�߿��������ͣ�������ѧ���ķ���������ʵ�������ͼ��������Ŀ��飬��Ŀ��Ҫ�漰�����ᴿ�ķ������������ʵķ���Ӧ�õ�֪ʶ���Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
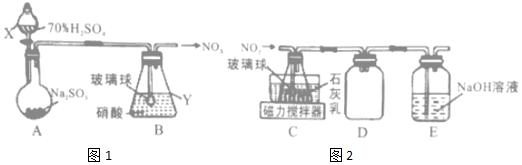
 ��ˮMgBr2������������ʵ���Ҳ���þм��Һ��Ϊԭ���Ʊ���ˮMgBr2��װ����ͼ���г�������ȥ������Ҫ�������£�
��ˮMgBr2������������ʵ���Ҳ���þм��Һ��Ϊԭ���Ʊ���ˮMgBr2��װ����ͼ���г�������ȥ������Ҫ�������£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������ɫƿ�� | B�� | ���ӷ� | C�� | ��ͭ����Ӧ | D�� | ���Ȳ��ֽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCHO | B�� | CH3COOCH2CH3 | C�� | HOOCCOOH | D�� | HCOOH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | CH3COOH | H2CO3 | HNO2 |
| ���볣�� | K=1.8��10-5 | K=4.3��10-7 K=5.6��10-11 | K=5.0��10-4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D | |
| ��Ʒ���� |  ̫���ܵ�� |  ʳ���� |  84����Һ |  �ϳ���ά��� |
| ���� ��Ҫ�ɷ� | SiO2 | �������� | ����� | �߷��Ӳ��� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com