
| A£® | Ō×Ó°ė¾¶£ŗY£¼Z£¼W | |
| B£® | µ„ÖŹµÄ»¹ŌŠŌ£ŗY£¼Z | |
| C£® | ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗX£¾W | |
| D£® | YŗĶZĮ½Õß×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ²»ÄÜĻą»„·“Ó¦ |
·ÖĪö ¶ĢÖÜĘŚŌŖĖŲX”¢Y”¢Z”¢WµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬XŌ×Ó×īĶā²ćµē×ÓŹżŹĒµē×Ó²ćŹżµÄČż±¶£¬ŌņXĪŖOŌŖĖŲ£»YÓėXæÉŠĪ³ÉY2X2ŗĶY2XĮ½ÖÖĄė×Ó»ÆŗĻĪļ£¬YĪŖNaŌŖĖŲ£»ZŌ×ÓµÄŗĖĶāµē×ÓŹż±ČYŌ×Ó¶ą2£¬ZĪŖAl£¬WÓėXĶ¬Ö÷×壬WĪŖSŌŖĖŲ£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗÓÉÉĻŹö·ÖĪöæÉÖŖ£¬XĪŖO£¬YĪŖNa£¬ZĪŖAl£¬WĪŖS£¬
A£®Ķ¬ÖÜĘŚ“Ó×óĻņÓŅŌ×Ó°ė¾¶¼õŠ”£¬ŌņŌ×Ó°ė¾¶£ŗY£¾Z£¾W£¬¹ŹA“ķĪó£»
B£®½šŹōŠŌŌ½Ē棬¶ŌÓ¦µ„ÖŹµÄ»¹ŌŠŌŌ½Ē棬Ōņµ„ÖŹµÄ»¹ŌŠŌ£ŗY£¾Z£¬¹ŹB“ķĪó£»
C£®·Ē½šŹōŠŌŌ½Ē棬¶ŌÓ¦Ēā»ÆĪļŌ½ĪČ¶Ø£¬Ōņ¼ņµ„ĘųĢ¬Ēā»ÆĪļµÄĪČ¶ØŠŌ£ŗX£¾W£¬¹ŹCÕżČ·£»
D£®YŗĶZĮ½Õß×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļ£¬·“Ӧɜ³ÉĘ«ĀĮĖįÄĘŗĶĖ®£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éŌ×Ó½į¹¹ÓėŌŖĖŲÖÜĘŚĀÉ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŌ×Ó½į¹¹”¢ŌŖĖŲµÄĪ»ÖĆĶʶĻŌŖĖŲĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėÓ¦ÓĆÄÜĮ¦µÄ漲飬עŅā¹ęĀÉŠŌÖŖŹ¶µÄÓ¦ÓĆ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĒįĖÉæĪĢƵ„ŌŖĘŚÖŠĘŚÄ©×ØĢā³å“Ģ100·ÖĻµĮŠ“š°ø
ĒįĖÉæĪĢƵ„ŌŖĘŚÖŠĘŚÄ©×ØĢā³å“Ģ100·ÖĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ėį | B£® | ¼ī | C£® | ŃĪ | D£® | Ńõ»ÆĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ģ¼ĖįĒāÄĘČÜŅŗÖŠ£ŗK+”¢SO42-”¢Cl-”¢Al3+ | |
| B£® | $\frac{{K}_{w}}{c£Ø{H}^{+}£©}$=1.0”Į10-13mol•L-1µÄČÜŅŗÖŠ£ŗNH4+”¢Ca2+”¢Cl-”¢NO3- | |
| C£® | ÓėAl·“Ó¦ÄܷųöH2µÄČÜŅŗÖŠ£ŗFe2+”¢K+”¢NO3-”¢SO42- | |
| D£® | ÓŠSO42-“ęŌŚµÄČÜŅŗÖŠ£ŗNa+”¢Mg2+”¢Ca2+”¢I- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ü¢Ž | B£® | ¢Ś¢Ū¢Ü | C£® | Č«²æ | D£® | ¢Ł¢Ü¢Ż¢Ž |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ²Ł×÷ | ĻÖĻó |
| Č”4g ĘÆ·Ū¾«¹ĢĢ壬¼ÓČė100mL Ė® | ²æ·Ö¹ĢĢåČܽā£¬ČÜŅŗĀŌÓŠŃÕÉ« |
| ¹żĀĖ£¬²āĘÆ·Ū¾«ČÜŅŗµÄpH | pH ŹŌÖ½Ļȱ䥶£ØŌ¼ĪŖ12£©£¬ŗóĶŹÉ« |
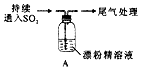 | 1£®ŅŗĆęÉĻ·½³öĻÖ°×Īķ£» 2£®ÉŌŗ󣬳öĻÖ»ė×Ē£¬ČÜŅŗ±äĪŖ»ĘĀĢÉ«£» 3£®ÉŌŗ󣬲śÉś“óĮæ°×É«³Įµķ£¬»ĘĀĢÉ«ĶŹČ„ |
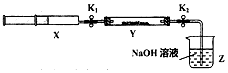
| ²Ł×÷²½Öč | ŹµŃéĻÖĻó | ½āŹĶŌŅņ |
| “ņæŖK1£¬ĶʶÆ×¢ÉäĘ÷»īČū£¬Ź¹XÖŠµÄĘųĢå»ŗĀżĶØČėY¹ÜÖŠ£Ø¼ŁÉč³ä·Ö·“Ó¦£© | £Ø1£©µ»ĘÉ«¹ĢĢå±äĪŖ°×É«·ŪÄ© | £Ø2£©·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗSO2+Na2O2=Na2SO4 |
| ½«×¢ÉäĘ÷»īČūĶĖ»ŲŌ“¦²¢¹Ģ¶Ø£¬“ż×°ÖĆ»Öø“µ½ŹŅĪĀ£¬“ņæŖK2 | £Ø3£©ZÖŠNaOHČÜŅŗµ¹ĪüČėY¹ÜÖŠ | £Ø4£©²»ÓĆ½āŹĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | AŗĶBµÄĻą¶Ō·Ö×ÓÖŹĮæÖ®²īĪŖ168 | |
| B£® | BŅ»¶Ø²»ÄÜ·¢Éś¼Ó³É·“Ó¦ | |
| C£® | ÓŠ»śĪļBÓėCH3CH2OH»„ĪŖĶ¬ĻµĪļ | |
| D£® | ·Ö×ÓŹ½ĪŖC5H10O2ĒŅÓėCH3COOHŹōÓŚĶ¬ĄąĪļÖŹµÄÓŠ»śĪļÖ»ÓŠ4ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 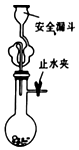 ŹµŃéŹŅÓĆ“óĄķŹÆŗĶŃĪĖįÖʱø¶žŃõ»ÆĢ¼ | |
| B£® | 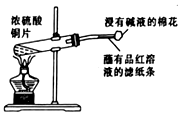 ÖĘČ”SO2”¢¼ģŃéSO2µÄĘư׊Ō | |
| C£® | 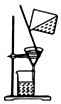 Ģį“æĒāŃõ»ÆĢś½ŗĢå | |
| D£® | 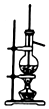 ŹµŃéŹŅÓĆŅŅ“¼ŗĶÅØĮņĖįÖĘŅŅĻ© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū¢Ü¢Ż | B£® | ¢Ł¢Ś¢Ū¢Ż | C£® | ¢Ł¢Ū¢Ü | D£® | ¢Ś¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĘųĢå×ÜÖŹĮæ±£³Ö²»±ä | B£® | ĻūŗÄZµÄĖŁĀŹÓėĻūŗÄXµÄĖŁĀŹĻąµČ | ||
| C£® | X”¢Y”¢ZµÄÅØ¶Č²»ŌŁ·¢Éś±ä»Æ | D£® | X”¢Y”¢ZµÄ·Ö×ÓŹżÖ®±ČĪŖ1£ŗ2£ŗ2 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com