
| A、50mL 12 mol?L-1浓盐酸与足量二氧化锰加热反应,转移电子数为0.3 NA |
| B、5.6 g铁与0.1 mol氯气充分反应转移电子数为0.3NA |
| C、1L1mol?L-1NaClO溶液中含有ClO-的数目为NA |
| D、60gSiO2晶体中含有硅氧键的数目为4 NA |


科目:高中化学 来源: 题型:

| A、温度T1℃比 T2℃高 |
| B、正反应为放热反应 |
| C、甲图纵轴可以表示A的转化率 |
| D、甲图纵轴可以表示混合气体平均相对分子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10 | B、12 | C、14 | D、21 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质的量浓度为1 mol/L的K2SO4溶液中,含2 NA个K+ |
| B、把40 g NaOH固体溶于1 L水中,所得溶液中NaOH的物质的量浓度为1 mol?L-1 |
| C、常温常压下,71 g Cl2含有2 NA个Cl原子 |
| D、标准状况下,11.2 L 氦气中含有的原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定温度、压强下,固体的体积只由其分子的大小决定 |
| B、一定温度、压强下,气体体积由其物质的量的多少决定 |
| C、等物质的量浓度的盐酸和硫酸中,H+的物质的量浓度相等 |
| D、气体摩尔体积是指1mol任何气体所占的体积为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:
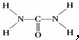 ,
,查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com