
 .
.分析 有A、B、C、D、E五种元素,A元素形成的-2价阴离子比氦的核外电子数多8个,则A的质子数为2+8-2=8,则A为氧元素;B元素的一种氧化物为淡黄色固体,该固体遇到CO2能生成A的单质,则B为Na元素,淡黄色固体为Na2O2;C为原子核内有12个中子的二价金属,当2.4gC与足量热水反应时,在标准状态下放出氢气2.24L,令C的相对原子质量为x,根据电子转移守恒,则$\frac{2.4g}{xg/mol}$×2=$\frac{2.24L}{22.4L/mol}$×2,解得x=24,故C的质子数为24-12=12,则C为Mg元素;D的M层上有7个电子,则D为Cl元素;E与A同周期且最外层比次外层多3个电子,最外层电子数为5,故E为N元素,据此解答.
解答 解:有A、B、C、D、E五种元素,A元素形成的-2价阴离子比氦的核外电子数多8个,则A的质子数为2+8-2=8,则A为氧元素;B元素的一种氧化物为淡黄色固体,该固体遇到CO2能生成A的单质,则B为Na元素,淡黄色固体为Na2O2;C为原子核内有12个中子的二价金属,当2.4gC与足量热水反应时,在标准状态下放出氢气2.24L,令C的相对原子质量为x,根据电子转移守恒,则$\frac{2.4g}{xg/mol}$×2=$\frac{2.24L}{22.4L/mol}$×2,解得x=24,故C的质子数为24-12=12,则C为Mg元素;D的M层上有7个电子,则D为Cl元素;E与A同周期且最外层比次外层多3个电子,最外层电子数为5,故E为N元素.
(1)C离子Mg2+,结构示意图为 ,故答案为:
,故答案为: ;
;
(2)A、E氢化物分别为H2O、NH3,由于非金属性O>N,故稳定性:H2O>NH3,故答案为:H2O>NH3;
(3)电子层结构相同的离子,核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径:Cl->O2->Na+>Mg2+,故答案为:Cl->O2->Na+>Mg2+;
(4)由C和D所组成的化合物为MgCl2,用电子式表示形成过程为: ,
,
故答案为: ;
;
(5)D单质与B的最高价氧化物对应水化物反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(6)Cu 与 E 的最高价氧化物对应水化物的稀溶液反应方程式:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,
故答案为:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O.
点评 本题考查结构性质位置关系的应用,推断元素是解题关键,注意元素周期律的理解掌握,熟练掌握元素化合物性质.


科目:高中化学 来源: 题型:选择题
| A. | 赤潮、白色污染、绿色食品中的“赤”“白”“绿”均指相关物质的颜色 | |
| B. | 为防止寨卡病毒传播,可用漂粉精或双氧水对环境进行消毒 | |
| C. | 大力开发利用可燃冰(固态甲烷水合物),有助于海洋生态环境的治理 | |
| D. | 硅酸钠溶液应存放在配有玻璃塞的广口试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | υ正=υ逆≠0时的状态 | B. | NO2全部转变成N2O4的状态 | ||
| C. | c(NO2)=c(N2O4)的状态 | D. | 体系的颜色发生变化的状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 )和双氧水为原料生产过氧化苯甲酰,写出合成过氧化苯甲酰的化学反应方程式:
)和双氧水为原料生产过氧化苯甲酰,写出合成过氧化苯甲酰的化学反应方程式: ,该反应属于取代反应.
,该反应属于取代反应.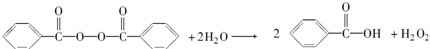 .苯甲酸的同分异构体中,属于酯类的有
.苯甲酸的同分异构体中,属于酯类的有 ,属于酚类的有3.(写结构简式)
,属于酚类的有3.(写结构简式)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Al>Mg>Na>H | B. | 热稳定性:NH3>PH3>H2S>HCl | ||
| C. | 元素非金属性:F>O>N>C | D. | 酸性:HClO4>H2SiO3>H3PO4>H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率通常用单位时间内反应物或生成物的质量变化来表示 | |
| B. | 化学反应速率的单位由浓度单位决定 | |
| C. | 在反应过程中,反应物的浓度逐渐变小,所以用反应物表示的化学反应速率为负值 | |
| D. | 用不同物质的浓度变化表示同一时间内、同一反应的速率时,其数值之比等于反应方程式中对应物质的化学计量数之比 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子化合物中都含有离子键 | |
| B. | 离子化合物中的阳离子只能是金属离子 | |
| C. | 离子化合物一定可以导电 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com