
| A. | 氯乙烷和水 | B. | 乙醇与水 | C. | 乙酸乙酯和乙醇 | D. | 漠苯与苯 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 记载中的反应属于置换反应 | B. | 记载中蕴含了湿法炼铜的原理 | ||
| C. | 由记载得出铁单质是赤色(红色) | D. | 每生成1mol铜转移2mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡含有添加剂的食物对人体健康均有害,不宜食用 | |
| B. | 硅胶可用作食品干燥剂 | |
| C. | “天宫一号”使用的碳纤维,是一种新型有机高分子材料 | |
| D. | 工业上燃烧煤时,加入少量石灰石是为了减少CO2的排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 目的 | 装置 | 原理 |
| A | 分离乙酸乙酯和乙醇 |  | 乙酸乙酯和乙醇的密度不同 |
| B | 实验室制备氨气 |  | 2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3+2H2O |
| C | 证明非金属性N>C>Si |  | 最高价含氧酸酸性:硝酸>碳酸>硅酸 |
| D | 除去丁醇中的乙醚 |  | 丁醇和乙醚的沸点不同 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
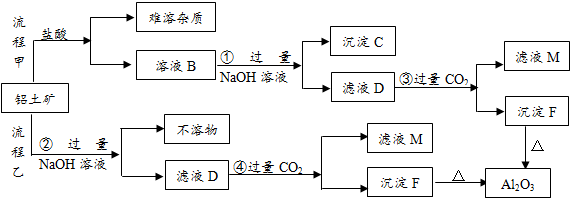
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
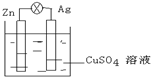 (1)在如图的银锌原电池中,银为正极,电极上发生的是还原反应(“氧化”或“还原”),电极反应式是Cu2++2e-═Cu.锌片上观察到的现象为锌片溶解,电极反应式为Zn-2e-═Zn2+.
(1)在如图的银锌原电池中,银为正极,电极上发生的是还原反应(“氧化”或“还原”),电极反应式是Cu2++2e-═Cu.锌片上观察到的现象为锌片溶解,电极反应式为Zn-2e-═Zn2+.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com