
| A. | 在相同条件下的溶解度:NaHCO3>Na2CO3 | |
| B. | 热稳定性:HF>HCl>HBr>HI | |
| C. | 氧化性:F2>Cl2>Br2>I2 | |
| D. | 碳酸钠溶液与稀盐酸互滴时,两种操作现象不相同 |
分析 A.相同条件下,碳酸氢钠的溶解度小;
B.元素的非金属性越强,其氢化物越稳定;
C.元素的非金属性越强,其单质的氧化性越强;
D.盐酸滴加碳酸钠中,首先生成HCO3-,所以没有气泡,盐酸过量时,H+进一步与HCO3-反应生成CO2;碳酸钠滴到盐酸中直接反应生成氯化钠和二氧化碳.
解答 解:A.Na2CO3和NaHCO3在相同条件下,碳酸氢钠的溶解度小,则在水中的溶解度为:Na2CO3>NaHCO3,故A错误;
B.元素的非金属性越强,其氢化物越稳定,非金属性:F>Cl>Br>I,则热稳定性:HF>HCl>HBr>HI,故B正确;
C.元素的非金属性越强,其氢化物越稳定,非金属性:F>Cl>Br>I,则氧化性:F2>Cl2>Br2>I2,故C正确;
D.盐酸滴加碳酸钠中,首先生成HCO3-,所以没有气泡,盐酸过量时,H+进一步与HCO3-反应生成CO2;碳酸钠滴到盐酸中直接反应生成氯化钠和二氧化碳,所以二者现象不同,故D正确.
故选A.
点评 本题考查碳酸钠和碳酸氢钠的性质、元素周期律,涉及溶解度、稳定性、与酸的反应、同主族元素性质的递变规律等,注意碳酸钠与酸反应时滴加顺序不同现象不同,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 测试时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能使广泛pH试纸显蓝色的溶液:K+、Na+、CH3COO-、Br- | |
| B. | 甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- | |
| C. | 0.1 mol?L-1 FeCl3溶液:K+、NH4+、I-、SCN- | |
| D. | 由水电离的c (H+)=1×10-14 mol?L-1的溶液中:Ca2+、K+、Cl-、HCO${\;}_{3}^{-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
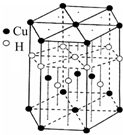 [Cu(NH3)4]SO4•H2O是一种杀虫剂.
[Cu(NH3)4]SO4•H2O是一种杀虫剂.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向次氯酸钙溶液中通入少量的二氧化硫:Ca2++3ClO-+SO2+H2O═CaSO4+2HClO+Cl- | |
| B. | 向偏铝酸钠溶液中通入少量的二氧化碳:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| C. | 向硅酸钠水溶液中通入少量的二氧化碳:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| D. | 向次氯酸钠溶液中通入少量的二氧化碳:ClO-+CO2+H2O═HClO+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①②③ | B. | 只有①② | C. | 只有②③ | D. | 只有①②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com