A
分析:A、标准状况下,三氧化硫不是气体;
B、甲基中的质子数等于电子数来分析;
C、氢氧化钡是强碱,在水溶液中可以完全电离;
D、乙烯与丙烯具有相同的最简式:CH
2,质量相同时,其原子数相同.
解答:A、标准状况下,三氧化硫不是气体,所以不能用22.4L/mol来计算其物质的量,故A错误;
B、甲基中的碳原子的质子数为6,氢原子的质子数为1,则碳原子含有6个电子,氢原子含有1个电子,总共是9个电子,即1mol甲基(-CH
3)中所含有电子数为9N
A,故B正确;
C、氢氧化钡是强碱,在水溶液中可以完全电离,1LpH=13的Ba(OH)
2溶液的物质的量为0.1mol,所以氢氧根的物质的量为0.1mol,即含有OH
-的数目为0.1N
A,故C正确;
D、乙烯与丙烯具有相同的最简式:CH
2,质量相同时,其碳原子数相同,为:
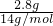
N
A=0.2N
A,故D正确.
故选A.
点评:本题是一道有关物质的量以及阿伏伽德罗常数的计算题目,难度不大.

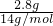 NA=0.2NA,故D正确.
NA=0.2NA,故D正确.

 阅读快车系列答案
阅读快车系列答案