
分析 (1)纤维素、淀粉都可以表示成(C6H10O5)n;
(2)纤维素、淀粉水解生成葡萄糖;葡萄糖中含-CHO,能利用银氨溶液或氢氧化铜悬浊液检验;
(3)碘单质遇淀粉变蓝色;葡萄糖中含-CHO,能利用氢氧化铜悬浊液检验;
(4)淀粉水解生成葡萄糖,葡萄糖遇碘水不变蓝,油脂在碱性条件下水解生成高级脂肪酸钠和甘油.
解答 解:(1)纤维素、淀粉都可以表示成(C6H10O5)n;
故答案为:淀粉或纤维素;
(2)纤维素、淀粉水解生成葡萄糖,则C6H12O6为葡萄糖,葡萄糖中含-CHO,能利用银氨溶液或氢氧化铜悬浊液检验,反应产生银镜或砖红色沉淀;
故答案为:葡萄糖;银氨溶液或氢氧化铜悬浊液;
(3)苹果中含有淀粉,碘单质遇淀粉变蓝色;苹果中含有葡萄糖,葡萄糖中含-CHO,能利用氢氧化铜悬浊液检验,产生砖红色沉淀;
故答案为:蓝;砖红色沉淀;
(4)A.馒头中含有淀粉,淀粉水解生成葡萄糖,葡萄糖有甜味,故A错误;
B.淀粉水解生成葡萄糖,葡萄糖遇碘水不变蓝,故B错误;
C.含有苯环的蛋白质遇浓硝酸变黄色,属于显色反应,不属于水解反应,故C正确;
D.油脂在碱性条件下的水解是皂化反应,故D错误.
故答案为C.
点评 本题考查有机物的性质,明确淀粉水解及葡萄糖的检验即可解答,题目难度不大,注重基础知识的积累.


科目:高中化学 来源: 题型:填空题

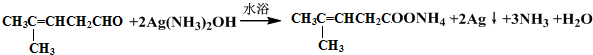
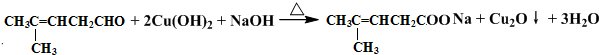 ;然后往反应后的溶液中加入稀硫酸至溶液呈酸性,再滴加足量的溴水,检验分子中碳碳双键,生成的有机产物的结构简式是
;然后往反应后的溶液中加入稀硫酸至溶液呈酸性,再滴加足量的溴水,检验分子中碳碳双键,生成的有机产物的结构简式是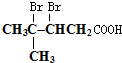 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘水,变蓝色;新制Cu(OH)2,砖红色沉淀;浓硝酸,变黄色 | |
| B. | 浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀;碘水,变蓝色 | |
| C. | 新制Cu(OH)2,砖红色沉淀;碘水,变蓝色;浓硝酸,变黄色 | |
| D. | 碘水,变蓝色; 浓硝酸,变黄色;新制Cu(OH)2,砖红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 大于0.2mol•L-1 | B. | 等于0.2mol•L-1 | C. | 小于0.2mol•L-1 | D. | 无法估算 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol 氢气和1 mol碘蒸气完全反应需要吸收26 kJ的热量 | |
| B. | 1个氢分子和1个碘分子完全反应需要吸收52 kJ的热量 | |
| C. | 1 mol H2(g)与1 mol I2(g)完全反应生成 2 mol的HI气体需吸收52 kJ的热量 | |
| D. | 1 mol H2(g)与1 mol I2(g)完全反应放出26 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
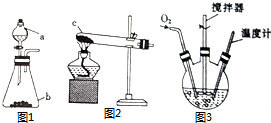 氯化亚铜(CuCl)是微溶于水但不溶于乙醇的白色粉末,溶于浓盐酸会生成HCuCl2,常用作催化剂.实验室可用废铜屑、浓盐酸、食盐及氧气制取CuCl.已知KMnO4不与稀盐酸反应,回答下列问题:
氯化亚铜(CuCl)是微溶于水但不溶于乙醇的白色粉末,溶于浓盐酸会生成HCuCl2,常用作催化剂.实验室可用废铜屑、浓盐酸、食盐及氧气制取CuCl.已知KMnO4不与稀盐酸反应,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
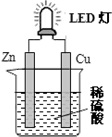
| A. | 锌片表面有气泡生成 | |
| B. | 装置中存在“化学能→电能→光能”的转换 | |
| C. | 如果将硫酸换成柠檬汁,导线中就不会有电子流动 | |
| D. | 如果将铜片换成锌片,LED灯仍然会发光 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

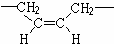 ,若顺丁橡胶的平均相对分子质量为540108,则平均聚合度为10002.
,若顺丁橡胶的平均相对分子质量为540108,则平均聚合度为10002.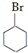 +NaOH$\stackrel{△}{→}$
+NaOH$\stackrel{△}{→}$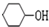 +NaBr.
+NaBr.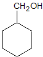 的合成路线.
的合成路线.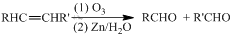 (R,R’代表烃基或氢)CH2=CHCH=CH2$\stackrel{催化剂}{→}$
(R,R’代表烃基或氢)CH2=CHCH=CH2$\stackrel{催化剂}{→}$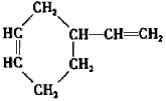

 $→_{催化剂}^{氢气}$
$→_{催化剂}^{氢气}$ .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com