
| ʵ�� | ʵ����� | ���� | ���� |
| �� | ����ˮ�м���̼�����Ʒ�ĩ | ����ɫ���ݲ��� | ������ˮ��Ӧ���ٲ�����һ������ǿ��̼������� |
| �� | ��Ʒ����Һ�е�����ˮ | ��Һ��ɫ | ������ˮ��Ӧ�IJ�����Ư���� |
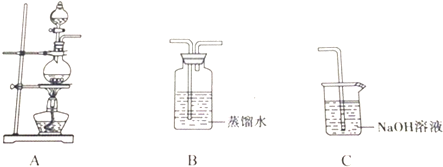
���� ��1���������̺�Ũ�����ڼ��������·�Ӧ�����������Ȼ��̺�ˮ��
��2����Ũ�����ӷ�����ȡ�����������Ȼ��⣬�����Ȼ����ܹ���̼�����Ʒ�Ӧ���ɶ�����̼��ã������������Ȼ����ڱ���ʳ��ˮ���ܽ��Բ�ͬ��ѡ����ӷ�����
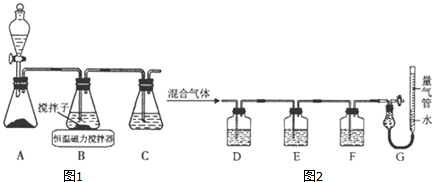
����֤������ˮ��Ӧ�IJ������Ư����Ӧ�����ų�����������Ӱ�죬��Ҫ���жԱ�ʵ�飻
�������������ܹ��������ӷ�Ӧ�����Ȼ�����ɫ��������ɫ������������������ʼ��������ӵĴ��ڣ�����Ԫ�ػ��ϼ۵��������жϱ�ͬѧ���ƶϣ�
����ȷ��ʵ��װ�úͲ�������ʵ�飬�۲쵽ʵ��������ʵ��������ƣ�˵����ˮ����Ư���Ժ����ԣ�
��3������������Һˮ��������ˮ��Ӧ�����Ȼ���ʹ����ᣬ����Cl2+H2O?H++Cl-+HClO�����ݻ�ѧƽ���ƶ�Ӱ�����ط������
��� �⣺��1���������̺�Ũ�����ڼ��������·�Ӧ�����������Ȼ��̺�ˮ������ѧ����ʽ��MnO2+4H++2Cl- $\frac{\underline{\;\;��\;\;}}{\;}$ Mn2++Cl2��+2H2O��
�ʴ�Ϊ��MnO2+4H++2Cl- $\frac{\underline{\;\;��\;\;}}{\;}$ Mn2++Cl2��+2H2O��
��2����Ũ�����ӷ�����ȡ�����������Ȼ��⣬�����Ȼ����ܹ���̼�����Ʒ�Ӧ���ɶ�����̼��Ҳ������ɫ���ݲ���������ˮ���ʼ�����ɸ��ţ�
�����ڱ���ʳ��ˮ���ܽ�Ȳ����Ȼ���������ˮ�����Կ�����ʢ�б���ʳ��ˮ��ϴ��ƿ��ȥ�Ȼ��⣻
�ʴ�Ϊ��HCl�� ��
��
��ʵ���û������֤�������������Ư���ԣ�����֤��������ˮ��Ӧ�IJ����Ƿ����Ư���ԣ�
�ʴ�Ϊ��Cl2��
���������ܹ��������ӷ�Ӧ�����Ȼ�����ɫ��������ɫ�������������ᣬ���Լ��������Ӵ��ڵķ�����ȡ������ˮ���Թ��У�������������ϡ���ᣬ���а�ɫ����������˵����Cl-���ڣ���ʵ���֪����ˮ�к�H+��Cl-����������ˮ��Ӧ������H+��Cl-���ȵĻ��ϼ۴���۽��͵�-1�ۣ���ȻҪ��Ԫ�ػ��ϼ����ߣ�H������ۣ��������ߣ�һ��������Ԫ�ػ��ϼ۵����ߣ�����Ԫ�ز�һ��ֻ���ߵ�+1�ۣ�
�ʴ�Ϊ��ȡ������ˮ���Թ��У�������������ϡ���ᣬ���а�ɫ����������˵����Cl-���ڣ�����ȷ����ʵ���֪����ˮ�к�H+��Cl-����������ˮ��Ӧ������H+��Cl-���ȵĻ��ϼ۴���۽��͵�-1�ۣ���ȻҪ��Ԫ�ػ��ϼ����ߣ�H������ۣ��������ߣ�һ��������Ԫ�ػ��ϼ۵����ߣ�����Ԫ�ز�һ��ֻ���ߵ�+1�ۣ�
����ȷ��ʵ��װ�úͲ�������ʵ�飬�۲쵽ʵ��������ʵ��������ƣ�˵����ˮ����Ư���Ժ����ԣ�
�ʴ�Ϊ�����Ժ�Ư���ԣ�
��3��������Һˮ��������ˮ��Ӧ�����Ȼ���ʹ����ᣬ����Cl2+H2O?H++Cl-+HClO����������ˮ��Һ�ӽ���ɫ��˵��c��Cl2����������Ϊ�㣬���������ı����Ȼ�����Һ����Һ����dz����ɫ��˵�������ӵļ�����������Cl2����������ˮ�ķ�Ӧ�ǿ��淴Ӧ������������Ũ�ȣ�ƽ����Ӧ�﷽���ƶ���ʹCl2���࣬���Գ���dz��ɫ��
�ʴ�Ϊ����������ˮ��Һ�ӽ���ɫ��˵��c��Cl2����������Ϊ�㣬���������ı����Ȼ�����Һ����Һ����dz����ɫ��˵�������ӵļ�����������Cl2����������ˮ�ķ�Ӧ�ǿ��淴Ӧ������������Ũ�ȣ�ƽ����Ӧ�﷽���ƶ���ʹCl2���࣬���Գ���dz��ɫ��
���� ���⿼����ʵ�����Ʊ������ķ�������ˮ�ɷּ����ʵ�ʵ��̽������ȷ�����Ʊ�ԭ������ˮ�ɷּ������ǽ���ؼ���ע��ʵ����������ԣ����ؿ���ѧ�������������������������Ŀ�Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �μ��˷�̪����Һ���ɫ | B�� | ���������ƶ�Na�ζ� | ||
| C�� | Na����ˮ�� | D�� | Na�۳ɹ���С�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
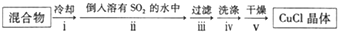
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
��| ��� | ���� | ��ѧ����ʽ |
| ʾ�� | ������ | H2WO3+3H3PO3�T3H3PO4+H2W�� |
| 1 | ��ԭ�� | H2SO3+Br2+2H2O�TH2SO3+2HBr |
| 2 | ���� | H2SO3+2NaOH�TNa2SO3+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | b-a=n+m | B�� | a-b=n+m | C�� | �˵������Y��X | D�� | ��������Y��X |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
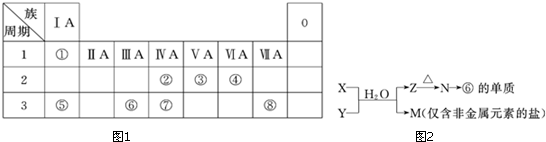
| A�� | R�ڻ���������+1�� | B�� | ����������ˮ����ļ��ԣ�X��R | ||
| C�� | ԭ�Ӱ뾶��W��R��X | D�� | R��Z�����γ����ӻ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Zn-2e-=Zn2+ | B�� | Br2+2e-=2Br- | C�� | 2Br--2e-=Br2 | D�� | Zn2++2e-=Zn |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com