
����Ŀ��һ���¶��£��������ݻ���Ϊ2.0 L�ĺ����ܱ������з�����Ӧ��
2NO(g)��2CO(g)![]() N2(g)��2CO2(g)
N2(g)��2CO2(g)
����������ʼ���ʵ����뷴Ӧ�¶����±���ʾ����Ӧ�����мס���������CO2�����ʵ�����ʱ��仯��ϵ��ͼ��ʾ��
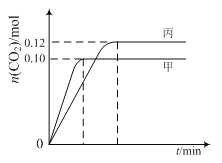
���� | �¶�/�� | ��ʼ���ʵ���/mol | |
NO (g) | CO (g) | ||
�� | T1 | 0.20 | 0.20 |
�� | T1 | 0.30 | 0.30 |
�� | T2 | 0.20 | 0.20 |
����˵����ȷ����
A. �÷�Ӧ������ӦΪ���ȷ�Ӧ
B. �ﵽƽ��ʱ������CO2����������ȼ��е�С
C. T1��ʱ������ʼʱ����г���0.40 mol NO��0.40mol CO��0.40mol N2��0.40mol CO2����Ӧ�ﵽ��ƽ��ǰv(��)��v(��)
D. T2��ʱ������ʼʱ����г���0.06mol N2��0.12 mol CO2�����ƽ��ʱN2��ת���ʴ���40%
���𰸡�CD
�����������������A.2NO(g)+2CO(g)N2(g)+2CO2(g)���ȹ���ƽ�¶ȸߣ���״̬�¶ȸ��ڱ���T1��T2����ʱ��ƽ��״̬������̼���ʵ���С��˵���¶�Խ��ƽ��������У��淴ӦΪ���ȷ�Ӧ������ӦΪ���ȷ�Ӧ����A����
B�����п��Կ����Ǽ���ʼ���ﵽƽ��״̬���ټ���0.1molNO��0.1molCO���൱������ƽ��ѹǿ��ƽ��������У��ﵽƽ��ʱ������CO2����������ȼ��еĴ�B����
C����״̬��ƽ��ʱCO���ʵ���Ϊ0.10mol��������м������ƽ�ⳣ����
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
��ʼ��(mol/L) 0.1 0.1 0 0
�仯��(mol/L) 0.05 0.05 0.025 0.05
ƽ����(mol/L) 0.05 0.05 0.025 0.05
K=![]() =10��
=10��
T1��ʱ������ʼʱ����г���0.40 mol NO��0.40mol CO��0.40mol N2��0.40mol CO2��Qc=![]() =2.5��K=10����Ӧ�ﵽ��ƽ��ǰv(��)��v(��)����C��ȷ��
=2.5��K=10����Ӧ�ﵽ��ƽ��ǰv(��)��v(��)����C��ȷ��
D��T2��ʱ��ƽ��״̬CO���ʵ���Ϊ0.12mol��
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
��ʼ��(mol) 0.2 0.2 0 0
ת����(mol) 0 0 0.1 0.2
�仯��(mol) 0.08 0.08 0.04 0.08
ƽ����(mol) 0.12 0.12 0.04 0.08
2NO(g)+2CO(g)![]() N2(g)+2CO2(g)
N2(g)+2CO2(g)
��ʼ��(mol) 0 0 0.06 0.12
ת���� 0.12 0.12 0 0
����ʼʱ����г���0.06mol N2��0.12 mol CO2����Ӧ������еõ�ƽ��״̬������ʼ��Ϊ0.12molNO��0.12molCO�ﵽ��ƽ����ͬ������ʼ��0.2molCO��NO��ȣ��൱�ڼ�����NO��CO0.08mol��CO��NO��ѹǿ��Сƽ��������У����Ե���ת���ʴ���40%����D��ȷ����ѡCD��


 ���źþ���Ԫ����ĩ��ϵ�д�
���źþ���Ԫ����ĩ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ʵ���Ũ����ͬ��������NaX��NaY��NaZ����Һ����pH����Ϊ8��9��10����HX��HY��HZ��������ǿ������˳����( )
A. HX��HY��HZ B. HX��HZ��HY
C. HZ��HY��HX D. HY��HZ��HX
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������йذ�����ε�˵������ȷ����
A��NH3�����������
B������ʪ��ĺ�ɫʯ����ֽ���鰱��
C��������ζ���ˮ������Һ������ʱ��c(NH4+) = c(Cl��)
D������ʱ��0.1mol��L��1NH4Cl��Һ��ˮϡ�ͣ�![]() ��ֵ����
��ֵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ������д��ȷ����( )
A��1����ԭ�� Na B��+2�۵���Ԫ�� Fe+2
C��4������� 4H D��3����������� 3NO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. ϡ�����ͭ�۷�Ӧ���Ʊ�����ͭ
B. �⻯����Ũ���ᷴӦ���Ʊ��⻯��
C. ���������������̼��Ӧ���Ʊ�����
D. ������������ȼ�տ��Ʊ���ˮ���Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������CO2�ĺ�������Ч���ã��Ѿ�����������ձ�����
��Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1L�ĺ����ܱ������У�����1mol CO2��3mol H2��һ�������·�����Ӧ��CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)��H=��49.0kJ/mol�����CO2��CH3OH(g)��Ũ����ʱ��仯��ͼ����ʾ��
CH3OH(g)+H2O(g)��H=��49.0kJ/mol�����CO2��CH3OH(g)��Ũ����ʱ��仯��ͼ����ʾ��
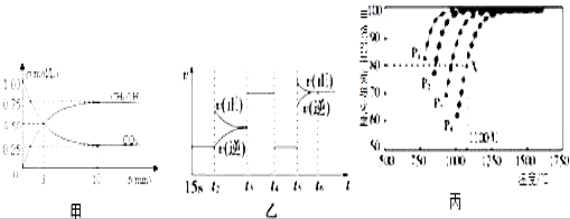
(1)ǰ3min�ڣ�ƽ����Ӧ����v(H2)=_________ _____�����¶��¸÷�Ӧ��ƽ�ⳣ��Ϊ____________(������λС��)��
(2)���д�ʩ�У�����ʹ��Ӧ�ӿ죬����ʹ![]() �������___________��
�������___________��
A�������¶� B������������� C����H2O(g)����ϵ�з��� D���ٳ���1mol H2
(3)ͼ����t5ʱ����ƽ���ƶ���������_____________��(�����)
A�������¶� B������Ӧ��Ũ�� C��ʹ�ô��� D��������ϵѹǿ
(4)��Ӧ�ﵽƽ�������Ӧ��ϵ�ټ���CO2(g)��H2(g)��CH3OH(g)��H2O(g)��1mol����ѧƽ��____________(�������������)�ƶ���
������CO2(g)+CH4(g) ![]() 2CO(g)+2H2(g)��CO2ת����ȼ������T��ʱ���ں����ܱ�������ͨ�����ʵ�����Ϊ0.1mol��CH4��CO2������������Ӧ�����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
2CO(g)+2H2(g)��CO2ת����ȼ������T��ʱ���ں����ܱ�������ͨ�����ʵ�����Ϊ0.1mol��CH4��CO2������������Ӧ�����CH4��ƽ��ת�������¶ȼ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
(5)������ʵ��˵���÷�Ӧ�ﵽƽ�����_______________
a��CO�����ʵ������ٷ����仯
b�����������ܶȲ��ٷ����仯
c��v��(CO2)=2v��(H2)
d���������ѹǿ���ٷ����仯
e����λʱ��������n mol CH4��ͬʱ����2n mol H2
(6)��ͼ��֪P1��P2��P3��P4��С�����˳����__________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������˵����ȷ����(����)
A. 0.1 mol Na2CO3��10H2O��������������������0.1NA
B. ���³�ѹ�£�18 mLˮ��������������ԼΪ10��7NA
C. ��״���£�22.4 L�����к��е�ԭ����ԼΪNA
D. 23 g���ΪC2H6O���л��C��H����ĿΪ3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ����(����)
A. ʯīϩ��ʯī��Ϊͬ��������
B. �����Ӳ֬��(C17H35COOH)��Ϊͬϵ��
C. ������������Ӧ���ɵõ��е㲻ͬ��3��һ�ȴ���
D. (CH3)3CCH2CH3��������2,2��������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com