
 2Z(g)其中X2、Y2、Z的起始溶度分别为0.10 mol/L、0.30 mol/L、0.20 mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )
2Z(g)其中X2、Y2、Z的起始溶度分别为0.10 mol/L、0.30 mol/L、0.20 mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是( )| A.c(Z)="0.50" mol/L | B.c(Y2)="0.50" mol/L |
| C.c(X2)="0.20" mol/L | D.c(Y2)="0.60" mol/L |
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:高中化学 来源:不详 题型:填空题
 CH3CH2OH(g)+3H2O(g)。
CH3CH2OH(g)+3H2O(g)。 | | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
 CH3OH(g)+ H2O(g)。2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L。下列判断不正确的是 。
CH3OH(g)+ H2O(g)。2min末该反应达到平衡,测得CH3OH的浓度为0.2mol/L。下列判断不正确的是 。
|
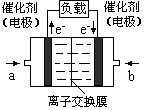
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(g) DH<0,反应过程中温度保持不变。已知起始时V乙
C(g) DH<0,反应过程中温度保持不变。已知起始时V乙
 V甲,装置如下图所示。当反应达平衡时,测得甲中C的体积分数为40%。下列说法中不正确的是
V甲,装置如下图所示。当反应达平衡时,测得甲中C的体积分数为40%。下列说法中不正确的是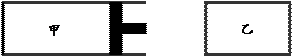
| A.容器甲、乙中反应的起始速率不等 |
| B.达平衡时,容器甲、乙中各组分的体积分数不等 |
| C.达平衡时,容器甲、乙中放出的热量相等 |
| D.达平衡时,容器乙中再充入少量稀有气体,A的转化率不变 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
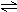 xC(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol/L。请填写下列空白:
xC(g),2min时反应达到平衡状态(温度不变),此时容器内剩余了0.8molB,并测得C的浓度为0.4mol/L。请填写下列空白: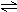 xC(g) ;△H =-QKJ/mol (Q>0)
xC(g) ;△H =-QKJ/mol (Q>0)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g) + D(s) ,可以判断反应达到平衡是( )
2C(g) + D(s) ,可以判断反应达到平衡是( )| A.单位时间内反应n molB,同时生成2n molC; | B.容器内气体的物质的量不再变化; |
| C.A的生成速率与B的生成速率相等;; | D.容器内气体的密度不再变化; |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2B(g),2B(g)
2B(g),2B(g) C(g)+2D(g)
C(g)+2D(g)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2O3,此时测知O2的转化率为30%,下列图象能正确表示气体的物质的量浓度(m)跟时间(t)的关系的是( )
2O3,此时测知O2的转化率为30%,下列图象能正确表示气体的物质的量浓度(m)跟时间(t)的关系的是( )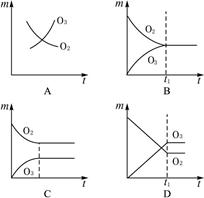
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g)(正反应为放热反应)达到平衡后,只改变一个条件时建立的新平衡的过程。填写下列各空(均填写图序号):
2NH3(g)(正反应为放热反应)达到平衡后,只改变一个条件时建立的新平衡的过程。填写下列各空(均填写图序号):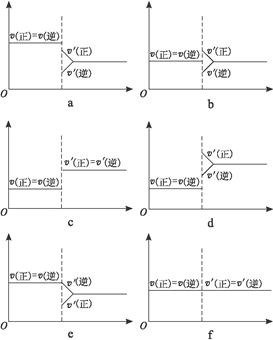
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
 2NH3(g);ΔH="-92.4" kJ·mol-1。请回答:
2NH3(g);ΔH="-92.4" kJ·mol-1。请回答: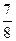 ,则N2的转化率a1= ,此时,反应放热 kJ;
,则N2的转化率a1= ,此时,反应放热 kJ;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com