
| ||
| ||
| 278a |
| 107 |
| 278a |
| 107 |


科目:高中化学 来源: 题型:
 如图是金属钨晶体中的
如图是金属钨晶体中的查看答案和解析>>
科目:高中化学 来源: 题型:
| A、读数时,俯视确定凹液面与刻度线相切 |
| B、容量瓶使用前经蒸馏水清洗后还残留有少量蒸馏水 |
| C、定容后把容量瓶颠倒摇匀,发现液面低于刻度线,又补足了所缺的水 |
| D、配制过程中,用蒸馏水洗涤烧杯和玻璃棒后,未把洗涤液移入容量瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
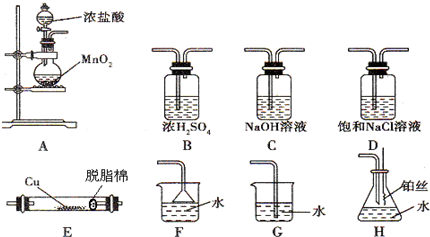
查看答案和解析>>
科目:高中化学 来源: 题型:
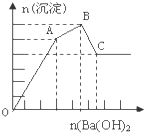 向FeCl3、Al2(SO4)3的混和溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如图所示.沉淀的生成与溶解的pH列于下表.以下推断错误的是( )
向FeCl3、Al2(SO4)3的混和溶液中逐滴加入Ba(OH)2(aq),形成沉淀的情况如图所示.沉淀的生成与溶解的pH列于下表.以下推断错误的是( ) | 氢氧化物 | 溶液PH | |||
| 开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
| Fe(OH)2 | 2.3 | 3.4 | - | - |
| Al(OH)2 | 3.3 | 5.2 | 7.8 | 12.8 |
| A、C点的沉淀为:Fe(OH)3和 BaSO4 |
| B、OA段可能发生的反应有:3Ba2++6OH-+3SO42-+Al3++Fe3+→3BaSO4↓+Fe(OH)3↓+Al(OH)3↓ |
| C、AB段可能发生的反应是:2SO42-+2Ba2++Al3++3OH-→2BaSO4↓+Al(OH)3↓ |
| D、据图计算原溶液中c(Cl-)=c(SO42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
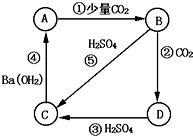 有A、B、C、D四种物质的溶液,在进行焰色反应实验时,火焰都呈黄色,它们之间可发生如图所示的转化,则这四种物质分别为:
有A、B、C、D四种物质的溶液,在进行焰色反应实验时,火焰都呈黄色,它们之间可发生如图所示的转化,则这四种物质分别为:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(O2)=3 mol?L-1?min-1 |
| B、v (SO2)=4 mol?L-1?min-1 |
| C、v (SO3)=0.1 mol?L-1?s-1 |
| D、v (O2)=0.1 mol?L-1?s-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com