
����Ŀ��������ѧ֪ʶ���ش��������⣮
��1��SiO2�Dz�������Ҫ�ɷ�֮һ��SiO2������������Һ��Ӧ�Ļ�ѧ����ʽΪ �� ����ʦ���������������ƣ�����̲�����
��2��������ͭ��Һ����μ���KI��Һ��ǡ�÷�Ӧ��ȫ���۲쵽������ɫ����CuI����ɫ��Һ��Ϊ��ɫ���÷�Ӧ�����ӷ���ʽΪ��ȡһ����������Ӧ����ϲ���ɫ��Һ��һ֧�Թ��У�����һ�����ı�������ʱ�۲쵽�������� ��
��3�����ӹ�ҵ����FeCl3��Һ��ʴ���ھ�Ե���ϵ�ͭ������ӡˢ��·�壬����ʦ��������ӡˢ��·��Ĺ�ҵ��ˮ�л���ͭ�������FeCl3��Һ��������·�����
�������ijɷ�Ϊ �� ���ѧʽ��
�ڼӹ���B������Ӧ�����ӷ���ʽΪ ��
��ͨ��C������Ӧ�Ļ�ѧ����ʽΪ ��
���𰸡�
��1��SiO2+2NaOH=Na2SiO3+H2O�������
��2��4I��+2Cu 2+=2CuI��+I2����Һ�ֲ㣬�ϲ���ҺΪ�Ϻ�ɫ
��3��Fe��Cu��Fe+2H+=Fe2++H2����Cl2+2FeCl2=FeCl3
���������⣺��1�������������������Ʒ�Ӧ���ɹ����ƺ�ˮ����ѧ����ʽ��SiO2+2NaOH�TNa2SiO3+H2O��������ܹ���������跴Ӧ�����ķ������ˮ���ܹ���ʴ��������������̲��������Դ��ǣ�SiO2+2NaOH�TNa2SiO3+H2O��������2��������ͭ��Һ����μ���KI��Һ��ǡ�÷�Ӧ��ȫ���۲쵽������ɫ����CuI����ɫ��Һ��Ϊ��ɫ˵����I2���ɣ���Ӧ����ʽΪ2CuSO4+4KI=I2+2CuI��+2K2SO4 �� ���ӷ���ʽΪ��4I��+2Cu 2+=2CuI��+I2 �� �������Ȼ�̼��ҺΪ�Ϻ�ɫ�������ܶȱ�ˮС�����Դ��ǣ�4I��+2Cu 2+=2CuI��+I2����Һ�ֲ㣬�ϲ���ҺΪ�Ϻ�ɫ����3����ȡ�����Ȼ�����Һ������A��������Һ���Ȼ�������Һ�������������������������ͭ����ȡ�����Ȼ������ܽ�����B����Ӧ�������ᣬ��ҺΪ�Ȼ��������Ȼ�������������Ӧ�����Ȼ���������CΪ�������������Ļ�ѧʽΪFe��Cu�����Դ��ǣ�Fe��Cu���ڼӹ������ᷢ����Ӧ�����ӷ���ʽΪFe+2H+=Fe2++H2�������Դ��ǣ�Fe+2H+=Fe2++H2�������ǽ������������������������ӣ���Ӧ����ʽ�ǣ�2FeCl2+Cl2=2FeCl3 �� ���Դ��ǣ�2FeCl2+Cl2=2FeCl3 ��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��T��ʱ��A������B���巴Ӧ����C���壬��Ӧ������A��B��CŨ�ȱ仯��ͼ������ʾ�������������������䣬�¶ȷֱ�ΪT1��T2ʱ��B�����������ʱ��Ĺ�ϵ��ͼ������ʾ�� 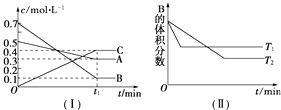
���������������ش��������⣺
��1��A��B��Ӧ����C�Ļ�ѧ����ʽΪ �� ����ӦΪ������ȡ����ȡ�����Ӧ��
��2�����ܱ������У�����2mol A��6mol B��
�ٵ���Ӧ�ﵽƽ��ʱ��A��B��Ũ�ȱ�����A��B��ת����֮���� ��
������ƽ����ϵ���¶ȣ�����������䣩����������ƽ����Է������� �� ����������С�����䡱��
�۵��ﵽƽ��ʱ�����������������ѹǿ���䣬ƽ�⽫������������������ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Һ���ڳ��������У���Һ���������ӵ���
A. Ũ���� B. ϡ���� C. Ũ���� D. Ũ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ȡ3.38g K2CO3��KHCO3�Ļ��������ˮ���25mL��Һ������Һ�м���25mL Ba��OH��2��Һǡ��ʹ���ɰ�ɫ����������࣮��Ӧ����Һ��c��OH����=0.8mol/L�����Ի�Ϻ���Һ����仯������ԭ�������K2CO3��KHCO3 ���ʵ���֮��Ϊ�� ��
A.1��2
B.1��1
C.2��1
D.2��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�������ܱ������У�һ�������·�����Ӧ��2A(?)B(g)��C(s)���ﵽ��ѧƽ��������¶ȣ�������������ܶ�����������������ȷ���ǣ� ��
A. ������Ӧ�����ȷ�Ӧ����AΪ����̬
B. ������Ӧ�Ƿ��ȷ�Ӧ����AΪ����̬
C. ��ƽ����ϵ�м�������C����ƽ�����淴Ӧ�����ƶ�
D. �ı�ѹǿ�Ը�ƽ����ƶ�һ����Ӱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��֤������ؾ����к�����Ԫ�أ�ѡ�ø������Լ��Ͳ����������˳����ȷ����
�ٵμ�AgNO3��Һ �ڼ�ˮ�ܽ� �۹��ˡ�ȡ��Һ ����������̻�ϼ��� �ݼ�ϡHNO3 ����Ũ���ᷴӦ ��NaOH��Һ���� ���õ��۵⻯��
A. �ܢڢۢ٢� B. �ޢ� C. �ޢߢ٢� D. �ڢ٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaCN����ĵ�Ʒ�ˮ��������������������
��.NaCN��NaClO��Ӧ������NaOCN��NaCl
��.NaOCN��NaClO��Ӧ������Na2CO3��CO2��NaCl��N2
��֪HCN��Ki=6.3��10��10���о綾��HCN��HOCN��NԪ�صĻ��ϼ���ͬ��
���������գ�
��1����һ������ʱ����Һ��pHӦ����Ϊ��ѡ����ԡ��������ԡ������ԡ�����ԭ���� ��
��2��д���ڶ�������ʱ������Ӧ�����ӷ���ʽ��
��3������100m3��NaCN10.3mg/L�ķ�ˮ��ʵ��������NaClOg��ʵ������ӦΪ����ֵ��4����������ʹNaCN��������0.5mg/L���ﵽ�ŷű���
��4����CN��2��Cl2�Ļ�ѧ�������ƣ���CN��2��NaOH��Һ��Ӧ��������H2O��
��5��������Ӧ�漰����Ԫ���У���ԭ�Ӻ������������ߵĵ����Dz�����H��C��N��O��Na��ԭ�Ӱ뾶��С�����˳��Ϊ ��
��6��HCN��ֱ���ͷ��ӣ�HCN�����ӣ�ѡ����ԡ��Ǽ��ԡ�����HClO�ĵ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���к͵ζ���ʼ��Ӧע�ӣ����ζ�����Һ��ı仯 ����ƿ����Һ��ɫ�ı仯 ���ζ�����Һ����������
A.������B.������C.������D.ֻ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������dz����ڵ��ƾ��в�ݮ�����ѡ�ӣ�ҡ�����������ζ��ʳ���㾫�����ķ���ʽΪC10H10O2 �� �ҷ�����ֻ����1��������������ֻ��һ��ȡ���������ĺ˴Ź�������ͼ����6���壬�����֮��Ϊ1��2��2��1��1��3�����ĺ����������ͼ�� 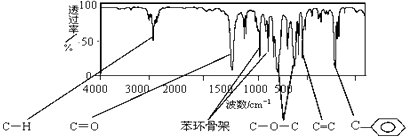
�Իش��������⣺
��1�����������Ľṹ��ʽ�� ��
��2��GΪ����������һ��ͬ���칹�壬����ӽṹģ����ͼ��ʾ 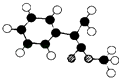 ��ͼ��������֮�����߱�ʾ������˫������
��ͼ��������֮�����߱�ʾ������˫������
�÷�����AΪԭ�Ϻϳ�G��·�����£�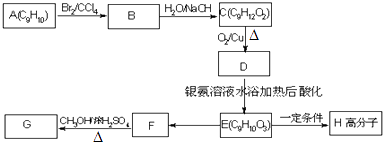
��֪��1molC��E���ʾ�������2mol�����Ʒ�Ӧ����������
�ڻ�����F��˳���칹�壮
��д��������E�еĹ��������������ƣ���
��A��B�ķ�Ӧ������ �� E��F�ķ�Ӧ������ ��
����д��ѧ����ʽ
C��D �� E��H ��
��E��C9H10O3����ͬ���칹���ж��֣�������һ�����ͨʽ��ʾ 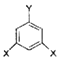 ������X��Y����ΪH������д����������ͨʽ���ܷ���������Ӧ�����Ȼ�����Һ������ɫ��Ӧ��2�����ʵĽṹ��ʽ ��
������X��Y����ΪH������д����������ͨʽ���ܷ���������Ӧ�����Ȼ�����Һ������ɫ��Ӧ��2�����ʵĽṹ��ʽ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com