
| A、稀盐酸 | B、稀硝酸 |
| C、硫酸铜溶液 | D、氢氧化钠溶液 |
科目:高中化学 来源: 题型:
| A、1.5 mol?L-1 |
| B、1 mol?L-1 |
| C、0.5 mol?L-1 |
| D、0.25 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向CuSO4溶液中加入钠:Na+Cu2+=Cu+Na+ |
| B、向Ba(OH)2溶液中滴加稀盐酸:2H++2Cl-+Ba2++2OH-=2H2O+BaCl2 |
| C、澄清石灰水与盐酸反应:H++OH-=H2O |
| D、往FeCl3溶液中加入Cu粉:2Fe3++3Cu=2Fe+3Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
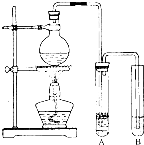 实验室制取少量溴乙烷的装置如图.
实验室制取少量溴乙烷的装置如图.查看答案和解析>>
科目:高中化学 来源: 题型:
A、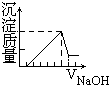 |
B、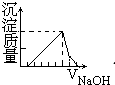 |
C、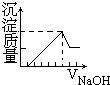 |
D、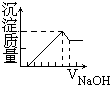 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | X | Y | Z | W | M | K | R | T | P |
| 原子半径/pm | 152 | 110 | 143 | 77 | 66 | 99 | 160 | 186 | 104 |
| 主要化合价 | +1 | -3,+5 | +3 | -4,+4 | -2 | -1,+7 | +2 | +1 | -2,+6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
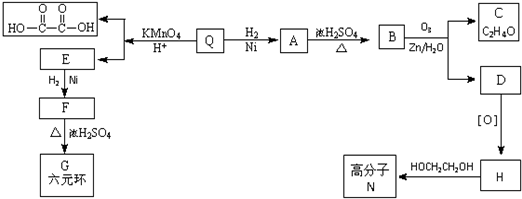
| KMnO4 |
| H+ |
| O3 |
| H2O/Zn |
查看答案和解析>>
科目:高中化学 来源: 题型:
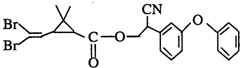 拟除虫菊酯是一类高效、低毒、对昆虫 具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊醋的结构简式如右图:下列对该化合物叙述正确的是( )
拟除虫菊酯是一类高效、低毒、对昆虫 具有强烈触杀作用的杀虫剂,其中对光稳定的溴氰菊醋的结构简式如右图:下列对该化合物叙述正确的是( )| A、属于芳香烃 |
| B、分子中含有4个手性碳 |
| C、含有3种官能团 |
| D、能发生取代、加成、加聚、氧化、消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com