
分析 (1)依据滴定实验和反应离子方程式,结合元素守恒计算得到;
(2)滴定实验误差分析依据标准溶液消耗的多少进行分析判断.
解答 解:(1)滴定反应为:Cu2++H2Y2-=CuY2-+2H+,铜离子物质的量和标准液物质的量相同:cmol/L×b×10-3L=bc×10-3mol;依据元素守恒可得:
20ml溶液中含有的CuSO4•5H2O物质的量为:bc×10-3mol,
则100ml溶液中含硫酸铜晶体的物质的量为:bc×10-3mol×$\frac{100ml}{20ml}$=5bc×10-3mol,
所以CuSO4•5H2O质量分数的表达式为:$\frac{cmol/L×b×1{0}^{-3}L×250g/mol×5}{ag}$×100%;
故答案为:$\frac{cmol/L×b×1{0}^{-3}L×250g/mol×5}{ag}$×100%;
(2)a.未干燥锥形瓶对实验结果无影响,故a错误;
b.滴定终点时滴定管尖嘴中产生气泡说明消耗标准液读数偏小,结果偏低,故b错误;
c.未除净可与EDTA反应的干扰离子,消耗标准液多,结果偏高,故c正确;
故答案为:c.
点评 本题通过制备硫酸铜晶体,考查了制备实验方案的设计,试题涉及硫酸铜晶体的制备方法、中和滴定的简单计算和误差的分析,题目难度中等,明确制备原理为解答本题关键,试题充分考查了学生的分析、理解能力及化学实验、化学计算能力.


科目:高中化学 来源: 题型:解答题
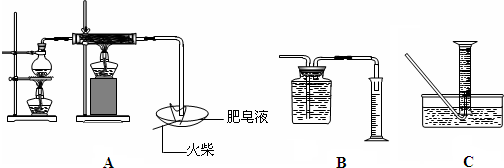
| 现象 | 结论与解释 | |
| 可能① | ||
| 可能② |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
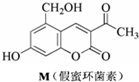
| A. | M与Br2可以发生取代反应,但不能发生加成反应 | |
| B. | M既能与FeCl3发生显色反应,也能与CH3COOH发生反应 | |
| C. | 1molM最多消耗3mol NaOH | |
| D. | 1molM在催化剂作用下最多能与5molH2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
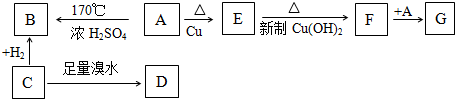
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C原子外围电子排布图: | B. | 硫原子结构示意图: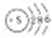 | ||
| C. | 二氧化硅的分子式:SiO2 | D. | 苯的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,C和E形成化合物的电子式
,C和E形成化合物的电子式 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验方案 |
| 1.用砂纸打磨后的镁带加适量水加热,再向反应后溶液中滴加酚酞 |
| 2.钠与滴有酚酞试液的冷水反应 |
| 3.镁带与2mol/L的盐酸反应 |
| 4.铝条与2mol/L的盐酸反应 |
| 5.向氯化铝溶液中滴加氢氧化钠溶液至过量 |
| 实验现象 |
| (A) |
| (B)反应不十分强烈,产生气体 |
| (C)剧烈反应,产生气体 |
| (D)生成白色胶状沉淀,然后沉淀消失 |
| (E)产生的气体可在空气中燃烧,溶液变成浅红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com