
| A. | 常温下金属A一定能与水反应,B一定不能与水反应 | |
| B. | A与B用导线连接后放入酒精中,一定形成原电池 | |
| C. | A与B用导线连接后放入B(NO3)2的溶液中,一定有电流产生 | |
| D. | 由A与B形成的原电池,A一定是负极,B一定是正极 |
分析 A、在金属活动顺序表中,排在前面的金属可以将后面的金属从其盐中置换出来;
B、根据构成原电池的条件来回答;
C、根据构成原电池的条件来回答;
D、在原电池中,负极金属的活泼性比负正金属的活泼性强.
解答 解:把金属A放入盐B(NO3)2的溶液中,发生如下反应:A+B2+═A2++B,则失去电子的是金属A,
A、金属Cu放入盐AgNO3的溶液中,发生铜置换银的反应:A+B2+═A2++B,但是金属铜和金属银和水都不反应,故A错误;
B、酒精属于非电解质,A与B用导线连接后放入酒精中,不能形成原电池,故B错误;
C、A、B用导线连接后放入B(NO3)2的溶液中,符合构成原电池的条件,有电流产生,故C正确;
D、由A与B形成的原电池,失电子的电极A一定是负极,B是正极,故D正确.
故选CD.
点评 本题涉及原电池的构成原理以及应用方面的知识,注意知识的梳理和归纳是解题的关键,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | KOH的电子式: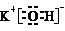 | |
| B. | S2-的离子结构示意图: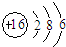 | |
| C. | 乙炔的分子式:C2H4 | |
| D. | 质子数为6、中子数为8的碳原子:${\;}_{6}^{8}$C |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
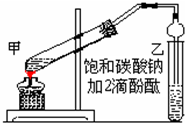 实验室制取乙酸乙酯的主要步骤如下:
实验室制取乙酸乙酯的主要步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2和H2在点燃或光照条件下合成氨 | |
| B. | 氨的稳定性比磷化氢弱 | |
| C. | 氨极易溶于水,氨水呈碱性,主要含 NH4+和OH- | |
| D. | 由氨制取硝酸铵的过程中,氨表现出还原性和碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| X | X+具有与Ne原子相同的电子层结构 |
| Y | 最外层电子数是次外层的一半,其最高正价与最低负价的绝对值相等 |
| Z | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| T | 元素单质的颜色是黄绿色的气体 |
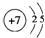 .
.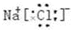 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 78gNa2O2固体中含有的阴离子数为2NA | |
| B. | 18g水中含有的电子数为10NA | |
| C. | 常温常压下,金属钠从水中置换出22.4LH2,发生转移的电子数小于2NA | |
| D. | 在1L2mol/L的硝酸铝溶液中含有的铝离子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由甲烷的氯代物有4种,可推知乙烷的氯代物有6种 | |
| B. | 乙烯和苯蒸气都能使溴水褪色,不能鉴别乙烯和苯蒸气 | |
| C. | 淀粉、油脂、蔗糖在一定条件下都能发生水解 | |
| D. | 乙烯和聚乙烯都能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将足量SO2通入含Fe2+、Cl-、Ba2+、Al3+的溶液中,四种离子仍能大量共存 | |
| B. | 向NaClO溶液中通入少量二氧化碳的离子方程式:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | 氢氧化铁与足量的HBr溶液反应的离子方程式:Fe(OH)2+3H+═Fe2++3H2O | |
| D. | 将100mL1mol•L-1的FeCl3溶液与足量NaS固体充分反应,生成沉淀10.4g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com