
ĪĀ¶ČĪŖT”ꏱ£¬Ļņ2.0 LŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė1.0 mol PCl5£¬·“Ó¦PCl5(g)
PCl3(g)+Cl2(g)¾¹żŅ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā”£·“Ó¦¹ż³ĢÖŠ²āµĆ²æ·ÖŹż¾Ż¼ūĻĀ±ķ£ŗ
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ £Ø £©
| A£®·“Ó¦ŌŚĒ°50 s µÄĘ½¾łĖŁĀŹv (PCl3) =" 0." 0032 mol”¤L-1”¤s-1 |
| B£®ĘäĖūĢõ¼ž²»±ä£¬ÉżøßĪĀ¶Č£¬“ļŠĀĘ½ŗāŹ±c (PCl3) =" 0." 11 mol”¤L-1 £¬Ōņ·“Ó¦µÄ”÷H<0 |
| C£®ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė2. 0 mol PCl3ŗĶ2. 0 mol Cl2 £¬“ļµ½Ę½ŗāŹ±£¬PCl3 µÄ×Ŗ»ÆĀŹŠ”ÓŚ80% |
| D£®ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė1. 0 mol PCl5”¢0. 20 mol PCl3ŗĶ0. 20 mol Cl2 £¬·“Ó¦“ļµ½Ę½ŗāĒ°v(Õż) > v(Äę) |
D
½āĪöŹŌĢā·ÖĪö£ŗA”¢ÓɱķÖŠŹż¾ŻæÉÖŖ50sÄŚ£¬”÷n£ØPCl3£©=0.32mol£¬v£ØPCl3£©= 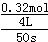 =0.0016mol/£ØL?s£©£¬¹ŹA“ķĪó£»
=0.0016mol/£ØL?s£©£¬¹ŹA“ķĪó£»
B”¢ÓɱķÖŠŹż¾ŻæÉÖŖ£¬Ę½ŗāŹ±n£ØPCl3£©=0.4mol£¬±£³ÖĘäĖūĢõ¼ž²»±ä£¬ÉżøßĪĀ¶Č£¬Ę½ŗāŹ±£¬c£ØPCl3£©="0.11" mol/L£¬Ōņn”ä£ØPCl3£©="0.11" mol/L”Į4L=0.44mol£¬ĖµĆ÷ÉżøßĪĀ¶ČĘ½ŗāÕżĻņŅĘ¶Æ£¬Õż·“Ó¦ĪŖĪüČČ·“Ó¦£¬¼“”÷H£¾O£¬¹ŹB“ķĪó£»
C”¢µČŠ§ĪŖĘšŹ¼¼ÓČė4.0molPCl5£¬ÓėŌĘ½ŗāĻą±Č£¬Ń¹ĒæŌö“ó£¬Ę½ŗāĻņÄę·“Ó¦·½ĻņŅĘ¶Æ£¬Ę½ŗāŹ±µÄPCl5×Ŗ»ÆĀŹ½ĻŌĘ½ŗāµĶ£¬¹ŹĘ½ŗāŹ±PCl3µÄĪļÖŹµÄĮæŠ”ÓŚ0.8mol£¬¼“ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė4.0 mol PCl3”¢ŗĶ4.0 mol Cl2£¬“ļµ½Ę½ŗāŹ±£¬PCl3µÄĪļÖŹµÄĮæŠ”ÓŚ0.8mol£¬²Ī¼Ó·“Ó¦µÄPCl3µÄĪļÖŹµÄĮæ“óÓŚ3.2mol£¬¹Ź“ļµ½Ę½ŗāŹ±£¬PCl3µÄ×Ŗ»ÆĀŹøßÓŚ80%£¬¹ŹC“ķĪó£»
D”¢¶ŌÓŚæÉÄę·“Ó¦£ŗPCl5£Øg£©?PCl3£Øg£©+Cl2£Øg£©£¬
æŖŹ¼£Ømol/L£©£ŗ0.5 0 0
±ä»Æ£Ømol/L£©£ŗ0.1 0.1 0.1
Ę½ŗā£Ømol/L£©£ŗ0.4 0.1 0.1
ĖłŅŌĘ½ŗā³£Źżk=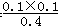 =0.025”£
=0.025ӣ
ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė2.0 mol PCl5”¢0.40 molPCl3ŗĶ0.40 molCl2£¬ĘšŹ¼Ź±PCl5µÄÅضČĪŖ0.5mol/L”¢PCl3µÄÅضČĪŖ0.1mol/L”¢Cl2µÄÅضČĪŖ0.1mol/L£¬ÅضČÉĢQc=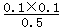 =0.02£¬K£¾Qc£¬ĖµĆ÷Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬·“Ó¦“ļĘ½ŗāĒ°v£ØÕż£©£¾v£ØÄę£©£¬¹ŹCÕżČ·£»¹ŹŃ”D”£
=0.02£¬K£¾Qc£¬ĖµĆ÷Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬·“Ó¦“ļĘ½ŗāĒ°v£ØÕż£©£¾v£ØÄę£©£¬¹ŹCÕżČ·£»¹ŹŃ”D”£
æ¼µć£ŗ»ÆŃ§Ę½ŗāµÄ¼ĘĖć
µćĘĄ£ŗ±¾Ģā漲鷓ӦĖŁĀŹ”¢Ę½ŗā³£Źż¼ĘĖć”¢Ę½ŗāŅĘ¶Æ”¢µČŠ§Ę½ŗāµČ£¬ÄѶČÖŠµČ£¬×¢ŅāDÖŠŹ¹ÓƵȊ§Ę½ŗāĖ¼Ļė·ÖĪö£¬Ź¹ĪŹĢā¼ņµ„»Æ£¬Ņ²æÉŅŌøł¾ŻĘ½ŗā³£Źż¼ĘĖć£¬µ«±Č½ĻĀé·³”£


 ŗ®¼Ł“ó“®ĮŖ»ĘɽŹéÉēĻµĮŠ“š°ø
ŗ®¼Ł“ó“®ĮŖ»ĘɽŹéÉēĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£Ø2012?½ĖÕ£©ĪĀ¶ČĪŖTŹ±£¬Ļņ2.0LŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė1.0mol PCl5£¬·“Ó¦PCl5£Øg£©=PCl3£Øg£©+Cl2£Øg£©¾¹żŅ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā£®·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄ²æ·ÖŹż¾Ż¼ūĻĀ±ķ£ŗ
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
£Ø2013?³¤ÄžĒųŅ»Ä££©ĪĀ¶ČĪŖTŹ±£¬Ļņ2.0LŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė1.0molPCl5£¬·“Ó¦PCl5£Øg£©?PCl3£Øg£©+Cl2£Øg£©¾Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā£®·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄ²æ·ÖŹż¾Ż¼ūĻĀ±ķ£ŗ
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĪĀ¶ČĪŖTŹ±£¬Ļņ2.0LŗćČŻĆܱÕČŻĘ÷ÖŠ³äČė2.0mol NO2£¬·“Ó¦2NO2£Øg£©?N2O4£Øg£©¾Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā£®·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄ²æ·ÖŹż¾Ż¼ūĻĀ±ķ£ŗ
|
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| W | X | Y | ||
| R | Z |
| t/s | 0 | 50 | 150 | 250 | 350 |
| n£ØPCl3£©/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
| t/s | 0 | 50 | 150 | 250 | 350 |
| n£ØPCl3£©/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A”¢·“Ó¦ŌŚĒ°50sµÄĘ½¾łĖŁĀŹĪŖv£ØPCl3£©=0.0032mol?L-1?s-1 |
| B”¢±£³ÖĘäĖūĢõ¼ž²»±ä£¬ÉżøßĪĀ¶Č£¬Ę½ŗāŹ±£¬c£ØPCl3£©=0.11mol?L-1£¬Ōņ·“Ó¦µÄ”÷H£¼0 |
| C”¢ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė1.0mol PCl5”¢0.20mol PCl3ŗĶ0.20mol Cl2£¬“ļµ½Ę½ŗāĒ°v£ØÕż£©£¾v£ØÄę£© |
| D”¢ĻąĶ¬ĪĀ¶ČĻĀ£¬ĘšŹ¼Ź±ĻņČŻĘ÷ÖŠ³äČė2.0mol PCl3”¢2.0mol Cl2£¬“ļµ½Ę½ŗāŹ±£¬PCl3µÄ×Ŗ»ÆĀŹŠ”ÓŚ80% |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com