
(16��) ���ȸʯ��һ�ֺ�ͭ��ʯ����ͭ��̬ΪCuCO3��Cu(OH)2��CuSiO3��2H2O��ͬʱ����SiO2��FeCO3��Fe2O3��Al2O3�����ʡ�����Ϊԭ����ȡ����ͭ�Ĺ���������ͼ��
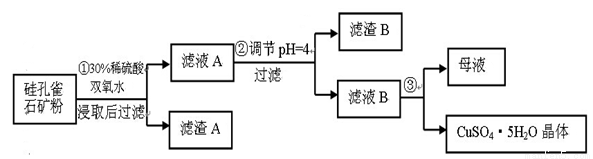
��1����ɲ������ϡ������CuSiO3��2H2O��Ӧ�Ļ�ѧ����ʽ��
CuSiO3��2H2O+H2SO4=CuSO4 +_______+H2O��˫��ˮ��������____ ��
��2������ڵ�����ҺpH������ѡ�õ��Լ���______��
A�� CuO B��Fe2O3 C��Al2O3 D��Cu(OH)2
��3���й��������↑ʼ��������ȫ������pH���±���
�������� | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
��ʼ������pH | 3.3 | 1.5 | 6.5 | 4.2 |
������ȫ��pH | 5.2 | 3.7 | 9.7 | 6.7 |
������У�����pH=4ʱ����������B�ijɷֵĻ�ѧʽΪ ����ҺB�г�Cu2+��, �����еĽ����������� ��
��4������ҺBͨ�� �� �����˵Ȳ����ɵõ�����ͭ���塣
��5���ⶨ����ͭ����ᾧˮ�ĺ���ʱ��Ӧ�������______�����ա�����ʧˮ�����ڿ�������ȴ�������ⶨ���____(�ƫ�ߡ�����ƫ�͡����䡱)��
(16��)��1��H4SiO4 (2��)����Fe2+ ������Fe3+ (2��)
��2�� AD��4��,ѡһ���Եĵ�2��,ȫ��4�֣���3��Fe(OH)3��Al(OH)3 (2�� ��1��) ��Al3+ (1��)
��4������Ũ������ȴ�ᾧ(2��) ��5������ (1��) �� ƫ�� (2��)
��������
�����������1�����������غ㶨�ɣ������ж�δ֪����ԭ���ᣬ���ù۲취��ƽ��Ӧ����ʽΪ��CuSiO3?2H2O+H2SO4��CuSO4+H4SiO4+H2O��˫��ˮ���������ԣ��ܰ��������������������ӣ�
��2��������ҺA��ʾ���ԣ�������Լ��ܹ��к���Һ�е������ӣ������������µ����ʣ�����Ӧ��ѡ������ͭ��������ͭ����ѡAD��
��3���б������ݿ�֪��pH��4ʱ��������������ȫ����������������������������Ҳ��ʼ�γ���������������������������B�ijɷֵĻ�ѧʽΪFe(OH)3��Al(OH)3��������������ȫ������Ҫ��pH��5.2������������û����ȫ�����������ҺB�г�Cu2+��, �����еĽ�����������Al3+��
��4����Һһ�����ͨ������Ũ������ȴ�ᾧ�����˵õ����壻
��5����������һ������������ɣ������ڿ�����ȴ����������³�����ʣ���������ƫ������ᾧˮ������ƫС�����ƫ�͡�
���㣺�����Թ��ȸʯΪԭ����ȡ����ͭ�Ĺ�������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����ӻ�������ܺ��й��ۼ� | B�������µ����������һ�������й��ۼ� | C�����ۻ������п��ܺ������Ӽ� | D���Ǽ��Է�����һ�������зǼ��Լ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡտ���и�����һ���¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����£���H2O2��Һ�еμ�����FeSO4��Һ���ɷ�������������Ӧ��2Fe2++H2O2+2H+��2Fe3++2H2O��2Fe3++H2O2��2Fe2++O2��+2H+������˵������ȷ����
A��H2O2�������Ա�Fe3+ǿ���仹ԭ�Ա�Fe2+ǿ
B����H2O2�ֽ�����У� Fe2+��Fe3+���������ֲ���
C����H2O2�ֽ�����У���Һ��pH���½�
D��H2O2��������Ҫ�ϸ�������Fe2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ�����и�����ѧ�ڵ�һ�νο��������Ծ��������棩 ���ͣ������
��16�֣���ʽ������[Fe(OH)SO4]��һ��������ˮ����������Ч����������ҽҩ��Ҳ���������������������Ѫ����ҵ�����÷���м�����������������������ȣ�������ʽ�������Ĺ����������£�
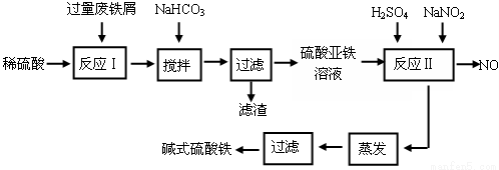
��֪������������������������ʽ����ʱ��Һ��pH���±���
������ | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
��ʼ���� | 2.3 | 7.5 | 3.4 |
��ȫ���� | 3.2 | 9.7 | 4.4 |
�ش��������⣺
��1����������NaHCO3��Ŀ���ǵ���pH�� ��Χ�ڣ�ʹ��Һ�е� ����(д���ӷ���)��
��2����Ӧ���м���NaNO2��Ŀ���� ��������Ӧ�����ӷ���ʽΪ ��
��3����ʵ�������У���Ӧ��ͬʱͨ��O2�Լ���NaNO2�������������뷴Ӧ��O2��11.2 L����״���������൱�ڽ�ԼNaNO2�����ʵ���Ϊ ��
��4����ʽ����������ˮ�������Fe(OH)2+���ӣ�Fe(OH)2+�ɲ���ˮ������Fe2(OH)42+ �ۺ����ӣ���ˮ�ⷴӦ�����ӷ���ʽΪ ��
��5����ҽҩ�ϳ����������������ᡢ����Ļ��Һ��Ӧ�Ʊ���ʽ�������������ҹ�����������Ʒ�в��ú���Fe2+��NO3����Ϊ�������ò�Ʒ���Ƿ���Fe2+��Ӧʹ�õ��Լ�Ϊ ��
A����ˮ B��KSCN��Һ C��NaOH��Һ D������KMnO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ�����и�����ѧ�ڵ�һ�νο��������Ծ��������棩 ���ͣ�ѡ����
���й��ڽ������仯�����������ȷ����
A��Fe��S��ϼ�������FeS2
B��������Cu��Ũ�������NO����
C��NaHCO3��Na2CO3��MgCO3���Ⱦ��ֽܷ���������
D��Na2O2��ˮ��Ӧ�����ȵ�Fe��ˮ������Ӧ���ܷ�Ӧ���ɼ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ�����и����ڶ��ε��п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
X��Y��Z��W��Ϊ����������Ԫ�أ���ͼΪ���ڱ���һ���֡�Wԭ�ӵ�����������������Ӳ�����2��������˵����ȷ����
| X |
| Y |
Z |
| W |
|
A��ͨ������£�XԪ��ֻ��������������
B��YԪ����̬�⻯��Ļ�ԭ����ǿ
C��XԪ�صķǽ����Ա�YԪ�طǽ�����ǿ
D��W������������Ӧˮ��������Ա�Z��ǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ�����и���9�µڶ����¿���ѧ�Ծ��������棩 ���ͣ������
��16�֣��Ͼ�����ӵ�ص��������ϣ���Ҫ����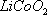 ������Al��Fe�ȣ������ڻ����ܡ�ﮣ�ʵ�鷽�����£�
������Al��Fe�ȣ������ڻ����ܡ�ﮣ�ʵ�鷽�����£�
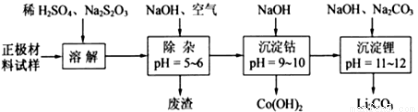
��֪��Fe3+��ʼ����pH=2.7, ��ȫ����pH=3.2; Al3+��ʼ����pH=3.8, ��ȫ����pH=5.2; Co2+��ȫ����pH=9.15
��1���������ܽ�����У�S2O32-��������SO42-,LiCoO2���ܽ�����з�Ӧ�Ļ�ѧ����ʽΪ ����������_________________________________��
��2�����������ӹ����У�ͨ�������������_____________________��ͨ������ͼ���NaOH��Һ���������ӷ���ʽ��______________ ��������Ҫ�ɷ���Al (OH)3��_______________��
��3���������ܡ��͡�����ﮡ������ӷ���ʽ�ֱ�Ϊ_________________��_________________��
��4���ù��տɻ��յĸ���Ʒ��_________________________��д��ѧʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ�����и�����ѧ�����п������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
������ѧϰ���о�����Ҫ˼ά�������������ƽ�����ȷ����
| ��ѧ��ʵ | ���ƽ��� |
A | Al��O2��ȼ������Al2O3 | Fe��O2��ȼ��Ҳ����Fe2O3 |
B | pH=3������ϡ��1000����pH=6 | pH=6������ϡ��1000����pH=9 |
C | �õ������MgCl2�ķ���ұ������þ | �õ������NaCl�ķ�����ȡ������ |
D | ��SO2ͨ��BaCl2��Һ���������� | ��SO2ͨ��Ba(NO3)2��Һ��Ҳ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015��㶫ʡ��ɽ�и���9�¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ����
A����������H2S����ͨ������ͭ��Һ�У� H2S+Cu2+=CuS��+2H+
B����NO2����ͨ��ˮ�У�2NO2+H2O= NO3��+ NO��+2H+
C��ICl ��Cl2�Ļ�ѧ�������ƣ���IClͨ��KOH��Һ�У�ICl+2OH��= I��+ ClO��+H2O
D����100ml 1.5mol/L��FeBr2 ��Һ��ͨ��0.15mol Cl2��2Br��+Cl2=Br2+2Cl��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com